无机纳米颗粒-独特性能及新应用
Professors Mark Asta1, Susan M. Kauzlarich2, Kai Liu3, Alexandra Navrotsky4, 1, Frank E. Osterloh2
1Departments of Chemical Engineering and Materials Science, 2Chemistry, 3Physics, 4Thermochemistry Facility and NEAT ORU, University of California, Davis
Material Matters Volume 2 Issue 1
简介
无机颗粒通常会具有新颖的物理性质,因为它们的尺寸接近纳米级尺寸。例如,纳米晶体量子点的独特电子和光学特性可能会导致其未来在电光设备和生物医学成像中的应用。1 对于从化学传感到磁记录的多种先进且多样化的应用,当前的研究越来越集中于利用纳米颗粒的高表面积体积比作为组装复杂纳米材料的框架。包括核/壳纳米颗粒和多组分分级组装体的结构可表现出增强的性能和新功能,而这是由于化学上不同的纳米结构组分的紧密相邻而实现的。本文重点介绍了可在基于无机纳米粒子的材料中实现的多种结构和性能,并指出了在控制这些性能方面提出的突出基本问题。这些问题是在几个绝缘和金属纳米颗粒例证的框架内进行讨论的,而这些例证是来自加州大学戴维斯分校教员的跨学科合作研究,并通过环境农业和技术(NEAT)组织研究单位(http://neat.ucdavis.edu)中的纳米材料相互作用。
为了充分了解其独特结构和物理特性的起源,重要的是要必须注意到纳米颗粒与散装材料不同,不仅因为它们很小,而且因为大部分体积都在表面的“很近距离”之内(图1)。因此,它们能够承载表面涂层的“沉重负荷”,在结构和成分上均与本体不同的区域。这些可以是纳米颗粒结构本身的重排(松弛)部分,具有不同组成的固体外壳或水、无机或有机分子的吸附层。这些吸附层可用作“链接”以构建新型的层次结构。可以利用粒子、涂层及其邻近环境之间的结构、键合和界面相互作用的基本复杂性来为许多潜在应用获得独特的性能。
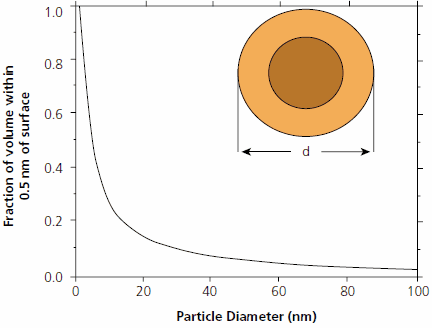
图 1.粒径在其表面0.5 nm以内的颗粒的体积分数。较轻的外壳代表该分数,或者在直径为d=1.5纳米的粒子上涂上0.5纳米涂层的体积。图由参考材料15修改得到。
复杂的多相材料
可视为氧化物纳米颗粒的各种结构和应用的第一个实例。以氧化铁和氢氧化物为例,首先要注意的是,这些物质存在于各种各样的多晶型中。2 常见的无水氧化铁是赤铁矿,a-Fe2O3,是一种常见的铁矿和红色颜料。磁铁矿,Fe3O4,是一种尖晶石,形成了众多磁性材料和器件的基础,而g-Fe2O3磁铁矿则具有一种缺陷型的尖晶石结构。羟基氧化物包括针铁矿、纤铁矿、赤铁矿、水铁矿和绿锈。氧化物和羟基氧化物在自然界和在合成材料中通常都是由纳米颗粒组成的。不同大小的氧化铁颗粒作为磁性记录材料、铁流体、颜料、腐蚀产物,以及在环境中营养物质和污染物(重金属和放射性核素)的运输中起着重要的作用。磁铁矿和磁赤铁矿的磁性在生物应用中也引起很大的关注。然而,磁铁矿的易腐蚀性以及在其纳米颗粒表面永久附着生物分子的困难是这类应用的重大障碍。这些问题可以通过在磁性纳米颗粒上包被一层外壳来解决,外壳可以保护核心免受氧化和腐蚀,此外,它还提供了一个化学功能化的平台,从而使这些颗粒具有潜在的生物相容性。例如,可以通过两个连续的反向胶束反应制备这种核/壳微粒。3
核/壳结构的磁性纳米颗粒目前是一系列广发应用的关注点。4 例如,由于可以进行远程磁操作,磁芯/Au壳结构的纳米颗粒可用于磁共振成像(MRI)、细胞标记和分类、热疗和靶向药物递送等生物学应用。5-7 迄今为止,已经报道了数种不同类型的磁性核/壳纳米颗粒,包括Fe/Au、Fe3O4/Au和FeCo/(Au,Ag)纳米颗粒。3,8-10 图2展示了一个Au涂层Fe纳米颗粒的离子。3,5,11,12 磁性硬/软核/壳纳米颗粒是另一种技术上重要的纳米结构。具有高磁晶各向异性的纳米颗粒,如L10相的FePt或CoPt,可以自组装成阵列,并作为未来具有Terabit/in2密度的图案磁性记录介质。13 磁芯/壳体结构将这种磁性硬相与磁性软相(如Fe3Pt)耦合,可用于实现用于永磁应用的大型能源产品。

图 2.(a) 通过扫描透射电镜得到的金包被的Fe纳米颗粒的Z -对比度图像。(b) 金包被的铁纳米颗粒的电子显微镜扫描图像。
在这些研究领域中,核/壳的结构、粒径、形状和表面性质是非常重要的。例如,对于使用每个高各向异性磁性纳米颗粒作为单比特位的磁记录应用程序,在尺寸和形状分布上的最小分散(<10%)是必不可少的。铁氧化物如Fe2O3、Fe3O4和MFe2O4(M=Fe, Co, Mn)可以制备成单分散表面衍生物纳米颗粒。14 在制备钴和铁纳米颗粒,以及用溶液法制备纳米棒方面也取得了进展。尽管有这些进步和令人兴奋的特性,核/壳结构纳米粒子仍面临巨大的合成挑战,尤其是在核/壳结构的生长机制和核/壳尺寸的独立控制方面。核/壳结构的详细表征,核和壳的优化以达到预期的性能,以及它们在生物学或技术上的应用还有待于系统的论证。
基础化学与物理学
以上这些应用均需要了解这些复杂纳米结构的基础物理学和化学。例如,表面和体积对粒子能量的贡献之间的竞争可以导致在纳米尺度上亚稳态的晶体结构(多晶)的热力学稳定。15-18 这种效应对这些无机材料的物理、化学、电子和磁性能的工程设计具有重要的影响。
实验量热学研究提供了铁氧化物和氢氧化物的表面能和水化能的数据。16 图3显示了在25 ºC下,不同的多晶型物相对于赤铁矿和液体的混合物组合的焓。可以看出,在大于15 m2/g的表面积上(由于熵的影响,甚至在更小的表面积上,针铁矿在自由能上也可能是稳定的),针铁矿相对于赤铁矿和水变得能量稳定。当表面积大于35 m2/g时,正方形铁矿相对于针铁矿变得稳定,纤铁矿是需要大于100 m2/g。当表面积大于250 m2/g时,正方形铁矿相对于针铁矿变得稳定。值得注意的是,无水相赤铁矿的焓和表面积(与表面能成比例)之间的关系曲线的斜率比任何水相都要高得多;这似乎也是氧化铝体系的一个普遍趋势。15-19 而且,亚稳态的多态性越高,其表面能越低,这一趋势不仅在氧化铁、氧化钛和氧化锆中存在,同样在氧化铁、氧化钛和氧化锆中也普遍存在。15 这些能量学上的复杂交叉现象可以解释氧化铁纳米颗粒在自然界和实验室中的合成和粗化行为。这些颗粒携带铅、铀等重金属或有机污染物的能力取决于其颗粒的晶体性质及其表面积。同样,磁性取决于相位和大小。

图 3.与粗赤铁矿加液态水½(Fe2O3 + H2O)相关的量热焓用于羟基氧化物和细粒赤铁矿与表面积(m2/g)的关系这些点表示实验数据,椭圆表示所研究的各种铁素体样品的范围。 图中总结了参考文献中的数据。16-18.

图 4.蒙特卡罗模拟快照(上图)显示了Fe-Pt纳米颗粒中平衡原子序跃迁的性质,其特征尺寸为4.79 nm。下方的图描绘了不同温度下纳米颗粒内部径向距离的有序参数分布图,表明了表面诱导的无序转变。上方的面图是从以下参考文献中重印的20,经过了Elsevier的许可。
除了为构建“相图”,以预测平衡态纳米颗粒结构随其大小变化的函数提供了框架外,所测热能也为表面结构和热力学的计算结果提供了直接的基准。原子级别的计算机模拟越来越多地应用于获得控制无机纳米颗粒结构转变和稳定性的热力学和动力学因素的详细信息。图4展示的是一个来自近期的FePt纳米粒子的蒙特卡洛模拟的示例。20 由于其异常大的磁各向异性能(MAE),以及超顺磁性的相关临界尺寸非常小,FePt化合物被认为是未来超高密度磁记录设备最有希望的候选材料之一。21 为了获得与其本体对应物相关的高MAE值,在其平衡四方相中形成FePt纳米颗粒至关重要(L10)。在合成过程中,FePt纳米颗粒一般在软磁性的亚稳立方(A1)相中形成,合成后需要一步退火步骤来诱导硬磁性四方相的形成。实验研究已表明立方四边形明显的尺寸依赖性,在具有纳米级直径的颗粒中显著下降的有序无序转变温度(TO)。22 计算机模拟表明,这种效应的起源是由于表面诱导的结构紊乱,从而在远低于TO本体值的温度下,颗粒被紊乱的表面区域“弄湿了”(图4)。这种表面诱导的无序性倾向受表面小面的晶体取向,以及Fe或Pt在颗粒表面上偏析程度的显著影响。这些结果表明,表面包被以及通过上述合成方法对颗粒形态的控制,是将高磁各向异性相控制到有序趋势且稳定的小尺寸颗粒的非常有效的方法。
表面包被和分层组件
表面包被也为化学组装更复杂的纳米结构提供了途径,例如用于高级应用的双组分结构。图5显示了具有光波导、磁致动器和化学传感器等潜在用途的离散双组分结构的例子。23 在第一个例子中(图5A),磁铁矿纳米颗粒与LiMo3Se3纳米线束共价连接,产生约400 nm长的针状结构。根据温度依赖的磁化测量,这些结构在长轴上呈现出磁各向异性,这是由于磁铁矿纳米颗粒之间的磁偶极相互作用造成的。因此,这种结构能够与弱磁场匹配,并起到纳米罗盘24或磁致动器的作用。图5B显示了一种由金纳米颗粒共价连接到由Ca2Nb3O10制成的胶体板的纳米结构。在这种结构中,纳米颗粒结构作为一个微尺度的镜子,能够将光反射到离散的方向。25 图中所示,是用两束激光照射这些分散的镜面样品所产生的红、绿、黄三色反射。另一种微型波导如图5C所示。在此处,六角形棒状氧化锌微晶体作为共价附着的CdSe纳米颗粒的载体。26 在紫外光照射下,所形成的微结构在杆端产生定向发射。这种发射来自于CdSe量子点的荧光,它是由ZnO微晶波导的。荧光的波长与CdSe纳米粒子的大小是可调的。图5B和C中的纳米结构应该引起空间光调制器、光学开关和发光器件方面的关注。最后一个例子说明了混合多组分纳米结构的潜在应用,静电结合SiO2-Au簇(图5D)可以用于纳米极性检测的定性和极性选择,或不同烃链长度的脂肪族硫醇(C2-C18)。27 与硫醇反应引起SiO2与Au颗粒结合的改变,导致簇的结构和颜色发生变化。由于这些传感器不需要其他组件来进行信号转导和处理,因此亚微米大小的簇是纳米级传感器的真实示例。

图 5. A. LiMo3Se3/Fe3O4纳米罗盘。B. Ca2Nb3O10/Au纳米镜子(插图:反射的光学显微图)。C. ZnO/CdSe光源发射器(插图:显示方向荧光的光学显微图)。D. SiO2/Au硫醇传感器(与十二烷基磺酸钠反应后)。
上述例子说明了材料的结构和性质在纳米尺度上可以发生巨大的变化,这些变化可以由热力学因素驱动,也可以由纳米颗粒成核和生长的动力学控制。复杂的分层纳米结构的组装,将走向新的材料和设备,取决于分子尺度上的相互作用,特别是在纳米颗粒的表面和界面的相互作用。对这些相互作用的基本理解需要实验和理论技术的结合,而对形成的纳米结构的表征则需要结构分析(电子显微镜和其他方法)和更大长度尺度的建模。在各种令人兴奋的应用前景的推动下,该领域的研究为开发这些方法并将其集成到从十分之一纳米到数千纳米的整体图像中提供了挑战。
参考文献
如要继续阅读,请登录或创建帐户。
暂无帐户?