Macmillan Imidazolidinonové organokatalyzátory
Asymetrická katalýza bez kovů
Organické katalyzátory na bázi imidazolidinonů, které vyvinul profesor David MacMillan na Caltechu, jsou určeny jako obecné katalyzátory pro různé asymetrické transformace. První vysoce enantioselektivní organokatalytický Dielsovu-Alderovu reakci s použitím (5S)-2,2,3-trimethyl-5-fenylmethyl-4-imidazolidinon monohydrochloridu uvedl MacMillan ve své průkopnické práci v roce 2000 (Snímek 1).1 Aktivovaný iminiový ion, který vznikl kondenzací imidazolidinonu a α,β-nenasyceného aldehydu, prošel reakcí s různými dieny za vzniku [4+2]-cykloaduktů s vynikajícími výtěžky a enantioselektivitou.
![Enantioselective Organocatalytic Diels-Alder Reaction Using (5S)-2,2,3-Trimethyl-5-Phenylmethyl-4-Imidazolidinone Monohydrochloride Reakce aktivovaného iminiového iontu, který vzniká kondenzací imidazolidinonu a α,β-nenasyceného aldehydu, s různými dieny za vzniku [4+2]-cykloaduktů s vynikajícími výtěžky a enantioselektivitou.](/deepweb/assets/sigmaaldrich/marketing/global/images/technical-documents/articles/chemistry-and-synthesis/reaction-design-and-optimization/enantioselective-organocatalytic/enantioselective-organocatalytic.jpg)
Schéma 1
Další organokatalytické transformace, jako jsou 1,3-dipolární cykloadice,2 Friedel-Craftsovy alkylace,
sup>3 α-chlorinace,3 α-fluorinace,42/sup> a intramolekulární Michaelovy reakce5 byly popsány s použitím MacMillanových imidazolidinonových organokatalyzátorů, přičemž všechny probíhaly s vysokou mírou enantioselektivity (Schéma 2).

Schéma 2
MacMillan našel optimalizovanou strukturu v (2S,5S)-(-))-2-tert-butyl-3-methyl-5-benzyl-4-imidazolidinon pro Friedelovu-Craftsovu alkylaci indolů (Schéma 3). 5,6
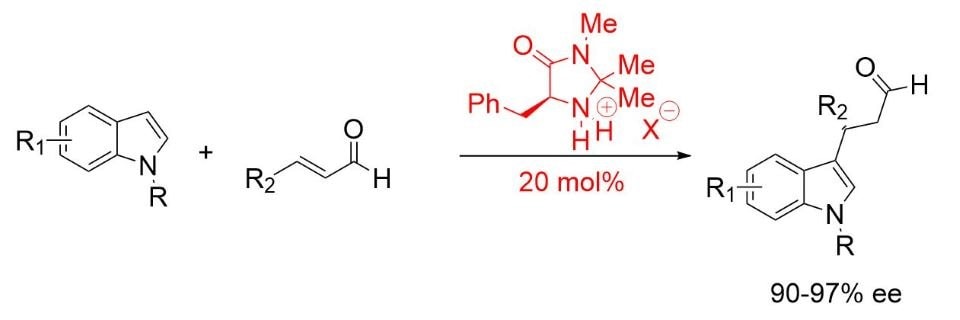
Schéma 3
Syntetická využitelnost této koncepce byla později prokázána při totální syntéze (-)-flustraminu B, biologicky aktivního alkaloidu obsahujícího pyrroloindolin (Schéma 4).7
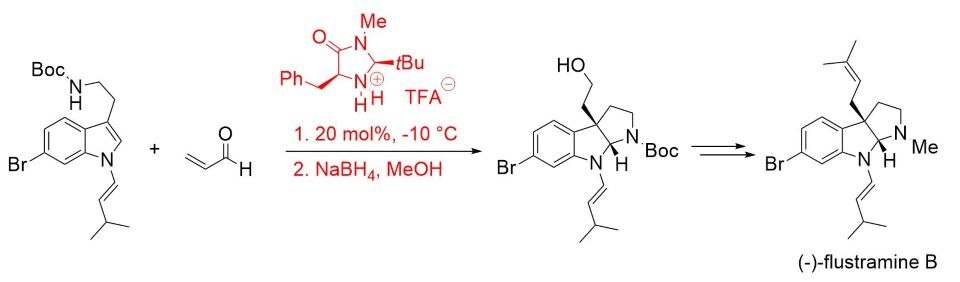
Schéma 4
Nedávno byl vyvinut fotochemický enantioselektivní α-alkylační protokol, který byl použit k úplné syntéze (-)-enterolaktonu a (-)-enterodiolu. Reakce probíhá v přítomnosti viditelného světla a za nepřítomnosti fotokatalyzátoru prostřednictvím světlem aktivovaného komplexu s přenosem náboje. (Schéma 5).8
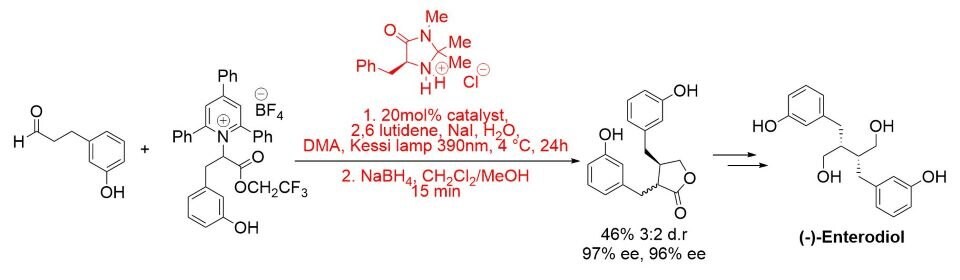
Schéma 5
Odkazy
Abyste mohli pokračovat ve čtení, přihlaste se nebo vytvořte účet.
Nemáte účet?