MSTFA/MSTFA-d9苯丙胺的衍生化,用于GC/MS检测和鉴定

以下内容来源于使用Sigma-Aldrich产品的外部资料。技术内容由以下人员撰写和提供:
Dieter Urbach, Bundeskriminalamt (BKA), KT 12 – Zentrale Analytik II, 65173 Wiesbaden, Germany
简介
衍生化,尤其是甲硅烷基化,通常用于气相色谱-质谱联用(GC-MS)来鉴定和定量已知和未知化合物。它不限于小分子,甚至肽也可被甲硅烷基化,特别是当需要引入氘时1。N-甲基-N-(三甲基硅烷基)三氟乙酰胺(MSTFA)是一种用途非常广泛的试剂,因为它可用于衍生化有机化合物中常见的许多官能团。它通过附着非极性三甲基硅烷基(TMS)基团起作用(图1)。在大多数情况下,TMS衍生物的沸点低于母体化合物,这使得能够在较低温度下进行GC分析。这降低了进样器或色谱柱中化合物热诱导衰变的可能性。对于定量分析,建议使用催化剂2-4。

图 1.羟基(甲硅烷基化)与MSTFA的反应,图中仅给出了醇(R-OH),但反应也适用于R-COOH、R = NH、R-NH2、R-SH
使用氘代MSTFA(MSTFA-d9)进行化合物鉴定
在某些情况下,尚不清楚精确地多少分子的官能团会受到衍生化反应的影响,尤其是在处理未知化合物时。使用氘代MSTFA(MSTFA-d9)有助于克服这个问题,因为对于每个衍生化的官能团,MSTFA-d9衍生物的分子量增加恰好9个质量单位。因此,可以通过考虑MSTFA/MSTFA-d9谱中的质量转移来计算原始化合物的分子量。
图2显示了在SLB™-5ms柱上使用GC-MS的安非他明(α-甲基苯乙胺)的质谱。伯胺和仲胺通常会产生 [M-1]+l 离子,其可能导致对分子量的错误解释和无法识别含氮化合物。安非他明还会产生非特异性和模糊的大片段;44 m/z可以匹配胺和醛(图2,上图)。在MSTFA衍生化后,质谱图(图2,中图)显示TMS衍生物的典型片段(TMS中甲基的丢失),而目标化合物安非他明可以基于片段质量192 m/z作为完整分子加以计算(192 + 15 m/z = 207m/z,TMS-安非他明)。
使用MSTFA-d9,192 m/z片段离子转移6个质量单位变至198 m/z,以及9个质量单位变至201 m/z(图2,下图)。第一个转移表示附着了一个TMS基团。9个质量单位的转移与安非他明结构的脂肪链中的甲基键断裂相关,其提供关于断裂机理的附加信息。

图 2.安非他明(上图)、TMS-安非他明(中图)和TMS-d9-安非他明(下图)的质谱图
图3显示了MSTFA衍生化对SLB-5ms气相色谱(GC)柱上所得色谱的影响。尽管样品中存在其他物质,但未衍生化的安非他明首先洗脱,然后是其TMS衍生物。该示例显示了如何使用衍生化方法来改变保留度或选择性,以查看通常可能与样品基质或样品的其他组分一起洗脱的未知化合物。
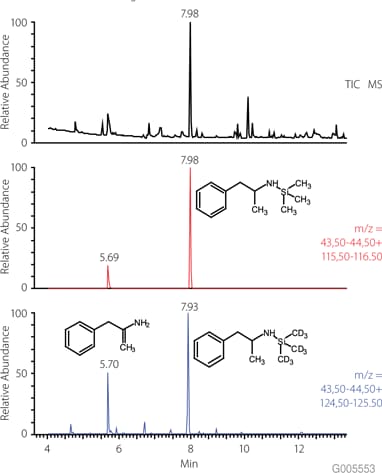
图 3.安非他明和TMS-安非他明的GC-MS色谱图(TIC,EIC)条件与图2相同。
总结
目前的大多数GC-MS系统都配备了质谱分辨率有限的单重四极杆质谱仪。它们不具备三重四极杆或离子阱质谱仪等获取MS/MS或MSn质谱的能力,这使得后者特别适合于本文所述的MSTFA/MSTFA-d9衍生化。不需要改变离子化技术,例如化学离子化,就能获得分子量或进行额外的MS/MS实验来了解片段或分子的结构和组成。
MSTFA和MSTFA-d9的另一个优点是其相应衍生物的色谱性质的可比性。TMS和TMS-d9衍生物在同一时间窗内洗脱。氘代化合物可能会早几秒钟洗脱出来。因此,即使在低浓度水平下,研究人员也可以凭借化合物保留时间来发现和鉴定目标化合物。
产品列表
参考文献
如要继续阅读,请登录或创建帐户。
暂无帐户?