Selectfluor™
Selectfluor™ (bis(tetrafluoroboran) 1-chlorometylo-4-fluoro-1,4-diazoniabicyklo[2.2.2]oktanu lub F-TEDA) jest przyjaznym dla użytkownika, łagodnym, stabilnym w powietrzu i wilgoci, nielotnym odczynnikiem do elektrofilowego fluorowania. Odczynnik Selectfluor™ jest w stanie wprowadzić fluor do substratów organicznych w jednym kroku, z niezwykle szerokim zakresem reaktywności.1 Wiele z tych reakcji wykazuje doskonałą regioselektywność.
Synteza silnego i niecytotoksycznego nukleozydowego inhibitora replikacji RNA wirusa zapalenia wątroby typu C została przeprowadzona przy użyciu odczynnika Selectfluor™ (Schemat 1). Ten rybonukleozyd wykazuje znacznie lepszy profil stabilności enzymatycznej w porównaniu do macierzystej 2'-C-metyloadenozyny.2
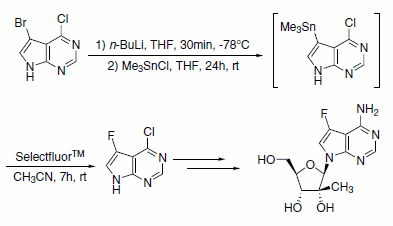
Schemat 1.
Fluorki allilowe mogą być otrzymywane na drodze sekwencyjnej metatezy krzyżowej/ elektrofilowej fluorodesililacji (Schemat 2). Ta droga pozwala uniknąć tworzenia się produktów ubocznych, które wynikają z transpozycji allilowej, co obserwuje się przy próbie nukleofilowego przemieszczenia lub reakcji otwarcia pierścienia z DAST.3
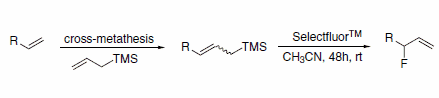
Schemat 2.
Odczynnik Selectfluor™ jest również zdolny do przeprowadzania innych transformacji. Jeden z przykładów wykorzystuje odczynnik Selectfluor™ jako alternatywę dla soli srebra lub rtęci w przegrupowaniu jodków do alkoholi (Schemat 3). W przypadku jodochlorku (X=Cl) podstawienie zachodzi tylko przy jodku, a nie chlorku.4
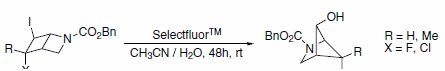
Schemat 3.
Odczynnik Selectfluor™ został użyty jako wydajny katalizator do przygotowania b-hydroksytiocyjanianów przy użyciu tiocyjanianu amonu w łagodnych warunkach (Schemat 4). We wszystkich przypadkach reakcje przebiegają szybko w temperaturze pokojowej bez tworzenia odpowiednich tiiranów, które są zazwyczaj wyłącznymi produktami, gdy stosowane są kwasy Lewisa, takie jak Sc(OTf)3 i InCl3 .5
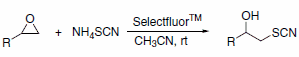
Schemat 4.
Referencje
Zaloguj się lub utwórz konto, aby kontynuować.
Nie masz konta użytkownika?Dla wygody naszych klientów ta strona została przetłumaczona maszynowo. Dołożyliśmy starań, aby zapewnić dokładne tłumaczenie maszynowe. Tłumaczenie maszynowe nie jest jednak doskonałe. Jeśli tłumaczenie maszynowe nie spełnia Twoich oczekiwań, przejdź do wersji w języku angielskim.