多肽合成
肽由兩個或兩個以上的氨基酸組成,以酰胺鍵連接,形成一條通常長 2 - 70 個氨基酸的氨基酸鏈。肽與蛋白質的區別在於,肽不需要折疊就具有生物活性。肽以肽荷爾蒙(如血管張力素、LHRH、腦蛋白)和毒素的形式存在於植物和動物中。縮氨酸作為藥物發現的先導化合物和藥物本身具有極大的興趣。多肽還應用於疫苗、生物材料、組織學探針,並大量用作產生抗體的抗原。
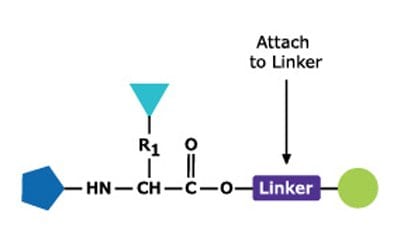
多肽是在溶液中或固相上化學合成的。該過程涉及在 N 保護氨基酸與帶有游離氨基和受保護羧酸的氨基酸之間定向和選擇性地形成酰胺鍵。在固相合成中,羧基保護基團會連結到聚合物支架上。鍵形成後,二肽的氨基保護基團會被移除,然後再接合下一個 N-保護胺基酸。
特色類別
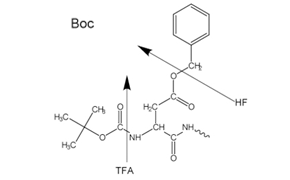
Figure 2Side-chain protecting groups for Boc solid-phase peptide synthesis (SPPS)
固相多肽合成(Solid-phase peptide synthesis,SSPS)因其高效、簡單、快速、易於平行化等優點,是最常用的多肽合成方法。SPPS 包括將氨基和側鏈保護的氨基酸殘基順序添加到附在 不溶性聚合物支持(圖 1)。
無論是酸性aboc基團(Boc SPPS)或鹼性aboc基團Fmoc-group(Fmoc SPPS)用於 N-α 保護。移除此保護基團後,使用偶合試劑或預先活化的保護胺基酸衍生物加入下一個保護胺基酸。C 端胺基酸會藉由連結劑,其性質決定了縮氨酸在鏈延伸後從支持物中釋放所需的條件。通常選擇側鏈保護基團,以便在多肽與樹脂脫離的同時被裂解(圖 2和3)。
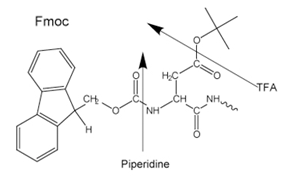
Figure 3.Side-chain protecting groups for Fmoc solid-phase peptide synthesis (SPPS)
相關文章
- Novabiochem® offers a wide range of linkers and derivatized resins for Fmoc solid-phase peptide synthesis with specialized protocols.
- 致色劑和致螢光劑衍生物是生物化學的寶貴工具,在酵素學、蛋白質化學、免疫學和組織化學方面有許多應用。
- Aspartimide formation 1,2 is caused by repeated exposure of aspartic acid-containing sequences to bases like piperidine and can result ultimately in the generation of 9 different by-products.
- Novabiochem® offers polymer supports for solid phase peptide synthesis, suitable for various peptide lengths and sequences.
- Long peptide purification removes impurities effectively, crucial for research and pharmaceutical applications.
- 查看全部 (16)
相關通訊協定
- A guide to create solvent systems used for the thin-layer chromatography assay of Novabiochem products.
- 利用含有半胱氨酸和蛋氨酸的 Fmoc 固相多肽合成協議,克服合成和二硫鍵形成的挑戰。
- 有关酰胺键和催化酰胺键形成协议的信息。胺和醇的酰胺化。酰胺键是有机化学中的重要键,是肽、聚合物以及许多天然产物和药物中的关键官能团。
- 無水 HF 是從 Boc 基樹脂裂解多肽的首選試劑,用途廣泛,對各種多肽合成非常有效。
- Fmoc 樹脂的裂解和脫保護是多肽合成的關鍵步驟,樹脂脫離後可得到所需的多肽。
- 查看全部 (13)
尋找更多文章和協議
How Can We Help
若有任何問題,請提交客戶支援請求
或與我們的客戶服務團隊討論:
電子郵件[email protected]
或致電 +1 (800) 244-1173
額外支援
- Chromatogram Search
Use the Chromatogram Search to identify unknown compounds in your sample.
- 計算機與應用程式
Web Toolbox - 用於分析化學、生命科學、化學合成和材料科學的科學研究工具和資源。
- Customer Support Request
Customer support including help with orders, products, accounts, and website technical issues.
- FAQ
Explore our Frequently Asked Questions for answers to commonly asked questions about our products and services.
若要繼續閱讀,請登入或建立帳戶。
還沒有帳戶?為便利客戶閱讀,此頁面中文以機器翻譯完成。雖然我們已盡力確保機器翻譯的準確性,但機器翻譯並非完美。如果您對機器翻譯的內容不滿意,請參考英文版本。
























