การวิเคราะห์ข้อมูล PCR/QPCR
- การวิเคราะห์เชิงคุณภาพ PCR/QPCR
- การวิเคราะห์ข้อมูล QPCR
- การหาค่า Cq ที่ถูกต้อง
- การตั้งค่าเกณฑ์ขั้นต่ำ
- กลยุทธ์การนับจำนวน QPCR
- ควอนตัมเส้นโค้งมาตรฐาน
- การเปรียบเทียบ/การเปรียบเทียบปริมาณ
- การทำให้เป็นปกติ
- การเลือกยีนอ้างอิง
- การวิเคราะห์ความเสถียรของยีนอ้างอิง
- วิธีการ Normalization ทางเลือก
- การวิเคราะห์ทางสถิติและการแสดงข้อมูล
- เทคนิคการสร้างภาพสำหรับการวิเคราะห์แบบสม่ำเสมอ
- Statistical Tests
- การจัดกลุ่มตามลำดับชั้น
- การวิเคราะห์ส่วนประกอบหลัก
การวิเคราะห์ข้อมูลเชิงคุณภาพ PCR/QPCR
หลังจากที่ PCR แบบดั้งเดิมเสร็จสมบูรณ์แล้วข้อมูลจะถูกวิเคราะห์ด้วยความละเอียดผ่านเจล agarose หรือเมื่อเร็วๆนี้ผ่านระบบอิเล็กโทรโฟเรซิสของหลอดเลือดฝอย สำหรับบางแอปพลิเคชัน qPCR จะทำงานพร้อมกับข้อมูลจุดสิ้นสุดที่ใช้สำหรับการวิเคราะห์เช่นสำหรับการพิมพ์ genotyping ของ SNP ในแต่ละกรณีข้อมูลปลายทางจะให้การวิเคราะห์เชิงคุณภาพหลังจากที่ PCR มาถึงช่วงหยุดนิ่งแล้ว ในบางกรณีอาจเป็นไปได้ที่จะวิเคราะห์ข้อมูลจุดสิ้นสุดเพื่อทำการวิเคราะห์กึ่งเชิงปริมาณของผลตอบแทน PCR แต่การวัดเชิงปริมาณมักทำโดยใช้ qPCR และการวิเคราะห์ค่าของรอบการวัดปริมาณ(Cq) 1 ค่า
การวิเคราะห์ข้อมูล QPCR
ตลอดคู่มือนี้ปัจจัยที่มีส่วนช่วยในการเปลี่ยนแปลงในการวัดกรดนิวคลีอิกโดยใช้ PCR หรือ qPCR จะได้รับการเน้น แต่ละปัจจัยเหล่านี้ควรได้รับการปรับให้เหมาะสมเพื่อให้ได้ผลในการวิเคราะห์ที่ให้ค่าที่ใกล้เคียงที่สุดกับปริมาณยีน (เป้าหมาย) จริงในปฏิกิริยา ผลลัพธ์ของกระบวนการเหล่านี้คือการสร้างชุด ค่า Cq สำหรับแต่ละเป้าหมายในแต่ละตัวอย่าง กระบวนการของการสร้างความเข้าใจและการวิเคราะห์ ค่า Cq เหล่านั้นเพื่อให้ข้อมูลที่เชื่อถือได้ซึ่งแสดงถึงเรื่องราวทางชีวภาพได้ถูกนำเสนอในบทนี้
การหา ค่า Cq ที่ถูกต้อง
การแก้ไขข้อมูลขั้นต้น
ค่า Cq จะถูกกำหนดสำหรับแต่ละชิ้นงานในแต่ละตัวอย่าง แพคเกจการวิเคราะห์ที่แตกต่างกันที่เกี่ยวข้องกับเครื่องมือที่แตกต่างกันมีวิธีการทางเลือกสำหรับการกำหนด Cq (และยังใช้ชื่อทางเลือกเช่น CT, CP, จุดออก) มันอยู่นอกเหนือขอบเขตของคู่มือนี้เพื่อเจาะลึกรายละเอียดของอัลกอริธึมเหล่านี้ทั้งหมด อย่างไรก็ตามการวัด qPCR ที่อิงตามเส้นโค้งการขยายจะไวต่อการเรืองแสงของพื้นหลัง การเรืองแสงพื้นหลังอาจเกิดจากปัจจัยหลายประการซึ่งรวมถึงการเลือกพลาสติกการเรืองแสงที่เหลืออยู่ของโพรบที่ไม่ดับแสงรั่วลงในตัวอย่างได้ดีและความแตกต่างในการตรวจจับด้วยแสงสำหรับแผ่นไมโครไทเตอร์ที่กำหนดได้ดี ในการวิเคราะห์ที่ได้รับการออกแบบมาเป็นอย่างดีพื้นหลังจะต่ำเมื่อเทียบกับสัญญาณขยาย อย่างไรก็ตามความผันแปรของสัญญาณพื้นหลังอาจเป็นอุปสรรคต่อการเปรียบเทียบเชิงปริมาณของตัวอย่างที่แตกต่างกัน ดังนั้นจึงเป็นสิ่งสำคัญที่จะต้องแก้ไขการเรืองแสงของพื้นหลังที่ทำให้เกิดความแตกต่างในเส้นฐาน (รูปที่ 10.1)

รูปที่ 10.1ส่วนประกอบของแผนการขยาย กราฟนี้แสดงการเพิ่มขึ้นของการเรืองแสงด้วยจำนวนรอบของตัวอย่างที่แตกต่างกัน ค่าเกณฑ์จะถูกตั้งค่าไว้สูงกว่าขีดจำกัดการตรวจจับแต่ต่ำกว่าระยะที่ราบสูงในระหว่างที่อัตราการขยายตัวช้าลง
วิธีการทั่วไปคือการใช้ความเข้มของการเรืองแสงในช่วงเริ่มต้นเช่นระหว่างรอบ 5 ถึง 15 เพื่อระบุองค์ประกอบคงที่และเชิงเส้นของการเรืองแสงของพื้นหลัง ซึ่งจะถูกกำหนดให้เป็นพื้นหลังหรือเส้นฐานสำหรับพล็อตการขยาย เนื่องจากผลกระทบชั่วคราวขอแนะนำให้หลีกเลี่ยงไม่กี่รอบแรก (เช่นรอบ 1 ถึง 5 สำหรับคำจำกัดความพื้นฐานเนื่องจากสิ่งเหล่านี้มักจะแสดงความคงตัวของปฏิกิริยา ยิ่งมีการใช้รอบในการแก้ไขค่าตั้งต้นมากเท่าใดความแม่นยำที่อาจเกิดขึ้นขององค์ประกอบเชิงเส้นของความแปรผันของค่าตั้งต้นก็จะยิ่งดีขึ้นเท่านั้น ชุดซอฟต์แวร์เครื่องมือจำนวนมากช่วยให้สามารถตั้งค่ารอบด้วยตนเองเพื่อใช้ในการกำหนดค่าพื้นฐานได้ ผู้ใช้ควรค้นหาฟังก์ชันเหล่านี้และต้องการยอมรับการตั้งค่าเริ่มต้นที่มีความทนทานอย่างยิ่ง
ตัวอย่างของผลกระทบของการตั้งค่าเบสไลน์แสดงอยู่ใน รูปที่ 10.1 ดังที่เห็นได้ ค่า Cq และรูปร่างที่ชัดเจนของพล็อตการขยายจะได้รับผลกระทบจากการตั้งค่าพื้นฐานที่ถูกต้อง ในตัวอย่างเส้นฐานของเส้นโค้งที่มีป้าย C3 ได้รับการปรับอย่างไม่ถูกต้องด้วยตนเองเพื่อให้รอบเส้นฐานคำนวณจากข้อมูลในรอบที่ 5 ถึงรอบที่ 31 ซึ่งจะทำให้เส้นโค้งลดลงทำให้ระดับเบสไลน์เป็นศูนย์ (รูปที่ 10 80 A) โดยมีค่า Cq เท่ากับ 2 28 ในการแก้ไขปัญหานี้ข้อมูลดิบ R จะถูกดูและรอบสุดท้ายของพื้นหลังแบบเส้นตรง (รอบสุดท้ายก่อนการขยาย) จะถูกระบุ ใน รูปที่ 10 2 Bสามารถดูได้รอบที่ 22 เส้นฐานจะถูกตั้งค่าให้เป็นศูนย์ระหว่างรอบ 52 และรอบ 22 (รูปที่ 10 2 องศาเซลเซียส) และเส้นฐานจะถูกแก้ไข (รูปที่ 10 มิติ) Cq ที่แก้ไข คือ 26 12 ดังนั้นโปรดสังเกตว่ามีความแตกต่างอย่างมากระหว่าง ค่า Cq กับการตั้งค่าข้อมูลขั้นต้นที่ไม่ถูกต้องและถูกต้องซึ่งแสดงให้เห็นว่าการตั้งค่าข้อมูลขั้นต้นที่ถูกต้องเป็นองค์ประกอบสำคัญของการวิเคราะห์ข้อมูล

รูปที่ 10 – 2 A – B ก)ตัวอย่างโดยทั่วไปของข้อมูลที่ลดลงต่ำกว่าค่าการอ่านค่าการเรืองแสงที่เป็นศูนย์เมื่อการตั้งค่าพื้นฐานไม่ถูกต้อง (พล็อตการขยายสีน้ำเงิน) b) ข้อมูลดิบของพล็อตการขยายเดียวกันที่แสดงขีดจำกัดของเส้นฐานเชิงเส้นและข้อมูลไม่ได้เป็นความผิดพลาด

รูปที่ 10 องศาเซลเซียส– 2 องศาเซลเซียส ค)ขีดจำกัดของการเริ่มต้นและสิ้นสุดของข้อมูลขั้นต้นจะถูกกำหนดโดยใช้การตั้งค่าซอฟต์แวร์ที่เหมาะสม d) การประยุกต์ใช้การตั้งค่าพื้นฐานที่ได้รับการแก้ไขส่งผลให้ได้ข้อมูลที่มีคุณภาพดี
การตั้งค่าเกณฑ์ขั้นต่ำ
แม้ว่านักวิจัยบางคนสนับสนุนการทำแผนที่พล็อตการขยายแต่ละบุคคลเพื่อประเมินประสิทธิภาพการขยายและปริมาณเป้าหมายในตัวอย่างที่วัดได้2,3,4 แต่วิธีการดั้งเดิมและที่พบมากที่สุดในการทำให้ Cq เป็นการใช้เกณฑ์ การใช้วิธีการนี้อย่างกว้างขวางมีแนวโน้มที่จะเกิดจากวิธีการเกณฑ์ที่เป็นวิธีการวัดปริมาณที่ง่ายและมีประสิทธิภาพ
หลักการที่อยู่เบื้องหลังวิธีการเกณฑ์คือเพื่อให้เห็นภาพสัญญาณฟลูออเรสเซนต์ที่เกี่ยวข้องจากการขยาย qPCR สัญญาณจะต้องเพิ่มขึ้นเพื่อให้อยู่เหนือขีดจำกัดการตรวจจับของเครื่องมือ (และดังนั้นเบสไลน์ รูปที่ 10.1) จำนวนรอบที่ต้องใช้ในการดำเนินการนี้จะเป็นสัดส่วนกับจำนวนสำเนาเริ่มต้นของชิ้นงานในตัวอย่าง ดังนั้นสัญญาณจึงต้องมีรอบการทำงานมากขึ้นเพื่อเพิ่มขึ้นสูงกว่าค่ามาตรฐานหากจำนวนสำเนาต้นฉบับเหลือน้อยและมีรอบการทำงานน้อยลงหากจำนวนสำเนามีค่าสูง เนื่องจากเส้นฐานถูกตั้งค่าไว้ที่ขีดจำกัดของการตรวจจับสำหรับระบบการวัดที่เส้นฐานจะไม่แม่นยำมาก ดังนั้นแทนที่จะวัดความเข้มของการเรืองแสงขั้นต่ำที่ระบบสามารถตรวจจับได้จะเลือกการเรืองแสงที่สูงขึ้นและมีการใช้เกณฑ์เทียม
การเลือกความเข้มของเกณฑ์ขั้นต่ำต้องยึดตามหลักการพื้นฐานบางประการ เป็นสิ่งสำคัญที่จะต้องตั้งค่าเกณฑ์ขั้นต่ำที่ความเข้มคงที่สำหรับชิ้นงานที่กำหนดและสำหรับตัวอย่างทั้งหมดที่จะนำมาเปรียบเทียบ หากมีตัวอย่างมากเกินไปที่จะใส่ลงในจานเดียวจะต้องใช้รูปแบบการปรับเทียบระหว่างแผ่นเช่นการรวมการควบคุมแบบจำลองที่ทำหน้าที่เป็นตัวควบคุมระหว่างแผ่นหรือการเจือจางแบบอนุกรมเส้นโค้งมาตรฐาน ในทางทฤษฎีสามารถตั้งค่าเกณฑ์ได้ทุกที่บนเฟสเชิงเส้นของเส้นโค้งการขยาย อย่างไรก็ตามในทางปฏิบัติเฟส Log-linear ของการขยายอาจถูกรบกวนจากการลอยของเบสไลน์เรืองแสงพื้นหลังเฟสที่ราบสูงหรือความแตกต่างในประสิทธิภาพการวิเคราะห์และดังนั้นการขยายการไล่ระดับสีของพล็อตที่รอบที่สูงขึ้น ขอแนะนำให้ตั้งค่าเกณฑ์ดังนี้:
- เหนือเส้นฐานเรืองแสงพื้นหลังอย่างเพียงพอเพื่อให้มั่นใจว่าจะหลีกเลี่ยงการขยายพล็อตข้ามเกณฑ์ก่อนกำหนดเนื่องจากการเรืองแสงพื้นหลัง
- ในขั้นตอนการบันทึกของพล็อตการขยายที่มันจะไม่ได้รับผลกระทบจากขั้นตอนที่ราบสูง (นี้จะเห็นได้ง่ายที่สุดโดยการดูแปลงขยายในมุมมองบันทึก รูปที่ 10 3 A)
- ในตำแหน่งที่ขั้นตอนของบันทึกของพล็อตการขยายทั้งหมดขนานกัน
แสดงกระบวนการตั้งค่าเกณฑ์ขั้นต่ำใน รูปที่ 10.3 ใน รูปที่ 10 3จุดขยายจะถูกดูบนสเกลล็อกแกน Y ดังนั้นจึงให้การขยายภาพของเฟสล็อกของการขยายและนำเสนอสิ่งนี้เป็นส่วนเชิงเส้นของพล็อตการขยาย เกณฑ์ขั้นต่ำจะถูกตั้งค่าที่ความเข้มของการเรืองแสงสูงสุด (โปรดดูที่แกน Y) ที่อยู่ภายในระยะบันทึกนี้และจุดที่แปลงการขยายทั้งหมดขนานกัน จากนั้นสเกลจะกลับไปยังมุมมองแบบเส้นตรง (รูปที่ 10 3 ข.) ซึ่งแสดงการตั้งค่าสูงสุดที่ตรงตามข้อกำหนดการตั้งค่าเกณฑ์ขั้นต่ำ หรืออาจตั้งค่าเกณฑ์ขั้นต่ำที่ปลายด้านล่างของระยะบันทึกนี้ (รูปที่ 10.3 10 และ 3 มิติ) ตราบใดที่ระยะการบันทึกของจุดขยายขนานกัน ΔCq ระหว่างตัวอย่างจะไม่ได้รับผลกระทบจากการตั้งค่าเกณฑ์ขั้นต่ำ

รูปที่ 10.3การตั้งค่าเกณฑ์จะมีผลต่อค่าสัมบูรณ์ Cq ที่บันทึกไว้และอาจมีผลต่อ ΔCq ระหว่างตัวอย่าง A). เมื่อใช้การลงจุดเชิงเส้นเทียบกับของข้อมูลเกณฑ์ขั้นต่ำจะถูกตั้งค่าที่ความเข้มสูงสุดของการเรืองแสงแต่จุดขยายจะแสดงระยะของการบันทึกแบบขนาน B). การตั้งค่าเกณฑ์ขั้นต่ำจะคงอยู่จาก A) และจะแสดงบนพล็อตแบบเส้นตรงและแบบเส้นตรง C). เมื่อใช้การลงจุดเชิงเส้นเทียบกับของข้อมูลเกณฑ์ขั้นต่ำจะถูกตั้งค่าที่ความเข้มของการเรืองแสงต่ำสุดแต่จุดขยายจะแสดงระยะของการบันทึกแบบขนาน D). การตั้งค่าเกณฑ์ขั้นต่ำจะคงอยู่จาก C) และจะแสดงบนพล็อตแบบเส้นตรงและแบบเส้นตรง ในแต่ละกรณีค่า ΔCq ระหว่างตัวอย่างจะเหมือนกัน
ข้อกำหนดสำหรับการตั้งค่าเกณฑ์ที่ตำแหน่งที่เฟสเชิงเส้นของการขยายสัญญาณจะขนานกันมากขึ้นเมื่อข้อมูลที่รอบสูงขึ้นถูกรวมอยู่ในการวิเคราะห์ ขั้นตอนการตั้งค่าเกณฑ์ขั้นต่ำที่อธิบายไว้สำหรับข้อมูลใน รูปที่ 10 3 ถูกทำซ้ำในชุดข้อมูลของ Cq ที่สูงขึ้น และผลลัพธ์ที่แสดงใน รูปที่ 10.4 ข้อมูล Cq ที่ได้ใน ตารางที่ 10 1 แสดงให้เห็นถึงความแปรปรวนใน Cqและที่สำคัญกว่า ค่า Δ Cq สำหรับสามแปลงขยายที่มีสามการตั้งค่าเกณฑ์ (รูปที่ 10.4) ค่า Δ Cq และค่าประมาณของปริมาณสัมพัทธ์ของชิ้นงานในแต่ละตัวอย่างจะขึ้นอยู่กับการตั้งค่าเกณฑ์ (รูปที่ 10.4) เป็นอย่างมากเนื่องจากการขยายไม่ขนานกัน

รูปที่ 10 4การวิเคราะห์ที่ดำเนินการและแสดงในรูปที่ 10.3 ถูกทำซ้ำโดยใช้ชุดข้อมูลอื่น ในกรณีนี้แผนการขยายไม่ขนานกันเนื่องจากความแตกต่างในประสิทธิภาพของปฏิกิริยาที่ Cq สูง การตั้งค่าต่ำสุดสำหรับ A) และ B) จะส่งผลให้ค่า ΔCq แตกต่างจากการตั้งค่าสูงสุดสำหรับ C) และ D) (สรุปไว้ในตารางที่ 10 1
กลยุทธ์การนับจำนวน QPCR
การตั้งค่าพื้นฐานและเกณฑ์ขั้นต่ำที่แม่นยำเป็นสิ่งจำเป็นสำหรับการวัดปริมาณที่เชื่อถือได้ หลังจากตั้งค่าแต่ละ ค่าแล้วค่า Cq จะถูกสร้างขึ้นและจะถูกใช้เป็นพื้นฐานสำหรับการหาปริมาณ จากนั้นปริมาณของชิ้นงานในตัวอย่างที่กำหนดจะถูกกำหนดโดยใช้เส้นโค้งมาตรฐานหรือการหาปริมาณสัมพัทธ์/เปรียบเทียบ
ควอนตัมเส้นโค้งมาตรฐาน
ตามที่ชื่อบอกเป็นนัยการวัดปริมาณเส้นโค้งมาตรฐานต้องใช้เส้นโค้งมาตรฐานเพื่อกำหนดปริมาณของชิ้นงานในตัวอย่างทดสอบ ปริมาณทั้งหมดที่กำหนดไว้สำหรับตัวอย่างจะสัมพันธ์กับปริมาณที่กำหนดให้กับเส้นโค้งมาตรฐาน ซึ่งต้องมีการใช้มาตรฐานภายนอกเพิ่มเติมควบคู่ไปกับปฏิกิริยาตัวอย่างทุกชุด ทางเลือกของวัสดุสำหรับเส้นโค้งมาตรฐานเป็นสิ่งสำคัญสำหรับการขจัดความแตกต่างที่อาจเกิดขึ้นในการวัดปริมาณเนื่องจากความแตกต่างระหว่างประสิทธิภาพการวิเคราะห์ในตัวอย่างและในมาตรฐาน ไซต์ที่มีผลผูกพันของไพรเมอร์ของมาตรฐานภายนอกจะต้องเหมือนกับไซต์ที่อยู่ในเป้าหมายมีลำดับที่เหมือนกับเป้าหมายมีความซับซ้อนที่คล้ายกันและได้รับการจัดการในลักษณะที่คล้ายกันมากที่สุดเท่าที่จะเป็นไปได้ ดังนั้นเมื่อวัดความเข้มข้นของเป้าหมายใน cDNA ขอแนะนำให้วัด cDNA เดียวกันในการเจือจางแบบอนุกรมของตัวอย่างควบคุม อย่างไรก็ตามสำหรับการศึกษาบางอย่างมีเหตุผลในทางปฏิบัติที่ป้องกันไม่ให้เกิดปัญหานี้ดังนั้นจึงเป็นสิ่งสำคัญที่จะทำซ้ำเงื่อนไขตัวอย่างให้ใกล้เคียงที่สุดเช่นโดยการเพิ่ม gDNA จากสายพันธุ์ที่ไม่เกี่ยวข้องกับสายพันธุ์ทดสอบไปยังมาตรฐาน oligonucleotide เทียมหรือ linearized plasmid ที่มีลำดับมาตรฐาน เมื่อระบุโครงสร้างหรือแอมพลิฟายเออร์ที่เหมาะสมแล้วเส้นโค้งมาตรฐานของการเจือจางแบบอนุกรมจะถูกสร้างขึ้น Cq สำหรับเป้าหมายจะถูกกำหนดสำหรับแต่ละมาตรฐานและลงจุดเทียบกับความเข้มข้นหรือค่าความเข้มข้น/การเจือจางสัมพัทธ์ในสเกลของปูมบันทึก ซึ่งจะส่งผลให้เกิดเส้นโค้งมาตรฐานที่ใช้ในการกำหนดความเข้มข้นของตัวอย่างทดสอบโดยการเปรียบเทียบ ค่า Cq ที่ได้จากการขยายตัวอย่างที่ไม่รู้จัก เมื่อใช้เส้นโค้งมาตรฐานสำหรับการวัดปริมาณการตั้งค่าเกณฑ์ขั้นต่ำจะต้องคงที่สำหรับการกำหนด Cq สำหรับมาตรฐานและสำหรับตัวอย่างบนแผ่นเดียวกัน เกณฑ์อาจแตกต่างกันระหว่างเพลท
การเปรียบเทียบ/การเปรียบเทียบปริมาณ
การหาปริมาณสัมพัทธ์หรือเปรียบเทียบจะใช้ความแตกต่างใน Cq เป็นดีเทอร์มีแนนต์ของความแตกต่างของความเข้มข้นของลำดับเป้าหมายในตัวอย่างที่แตกต่างกัน แทนที่จะวัดปริมาณของชิ้นงานต่อตัวอย่างเช่นเดียวกับวิธีเส้นโค้งมาตรฐานซึ่งจะนำไปสู่ชุดข้อมูลที่แสดงการเปลี่ยนแปลงการพับระหว่างตัวอย่าง
ในรูปแบบเดิมของวิธีการนี้5ประสิทธิภาพของการวิเคราะห์ทั้งหมดได้รับการสันนิษฐานว่าเป็นร้อยละ 100 นำไปสู่สมมติฐานที่ว่า ความแตกต่างของ Cq 1 (Δ Cq = 1) เป็นผลมาจากความแตกต่าง 2 เท่าของเป้าหมาย ในการกำหนดการเปลี่ยนแปลงพับในเป้าหมายหรือยีนที่สนใจ (GOI) ข้อมูลจะต้องถูกอ้างอิงไปยังการควบคุมการโหลด (ยีนอ้างอิงอ้างอิงอ้างอิงอ้างอิงอ้างอิง ; ดูต่อไปนี้สำหรับการอภิปรายเกี่ยวกับการทำให้ข้อมูลเป็นปกติ)
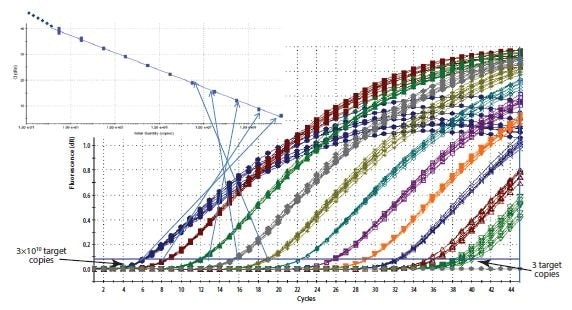
รูปที่ 10 5การสร้างเส้นโค้งมาตรฐาน Cq ที่บันทึกไว้สำหรับตัวอย่างแต่ละชุดของชุดการเจือจางจะถูกลงจุดบนสเกลลิเนียร์ล็อกเทียบกับความเข้มข้นสัมพัทธ์
ใน สมการ 1อัตราส่วนของ GOI หลังจากแก้ไขยีน ref ในตัวอย่าง 2 ตัวอย่าง (A สัมพันธ์กับ B) จะถูกวัดเป็น: 2 (สมมติว่าปฏิกิริยาที่มีประสิทธิภาพร้อยละ 100) ยกกำลังของความแตกต่างใน ค่า Cq สำหรับ GOI หารด้วย 2 ยกกำลังของความแตกต่างใน ค่า Cq สำหรับยีน ref

สมการ 1ต้นฉบับ (Livak) รุ่นการนับจำนวนสัมพัทธ์
อย่างไรก็ตามตามที่แสดงใน การเพิ่มประสิทธิภาพและการตรวจสอบการทดสอบประสิทธิภาพของปฏิกิริยาจะแตกต่างกันไปอย่างมากและอาจส่งผลกระทบอย่างมากต่อข้อมูล ดังนั้นสมมติฐานใน สมการ 1 จึง ได้รับการแก้ไข (สมการ 2)6เพื่อให้ความแตกต่างในประสิทธิภาพของปฏิกิริยาสามารถรวมเข้ากับการวิเคราะห์ได้ ในกรณีนี้ปัจจัยการขยาย 2 จะถูกแทนที่ด้วยประสิทธิภาพที่แท้จริงของ PCR (ตามที่กำหนดโดยการวิเคราะห์เส้นโค้งมาตรฐานดู การเพิ่มประสิทธิภาพและการตรวจสอบการวิเคราะห์การวิเคราะห์)

สมการ 2ประสิทธิภาพที่ปรับเปลี่ยน (Pfaffl) รุ่นการนับจำนวนสัมพัทธ์
เป็นตัวอย่างของการใช้ประสิทธิภาพที่ปรับ (สมการ 2) รูปแบบเชิงปริมาณสัมพัทธ์ชุดของ ค่า Cq จะแสดงใน ตารางที่ 10.2 ประสิทธิภาพของ GOI คือ 1.8 และสำหรับยีนอ้างอิง 1.94
นี่เป็นตัวอย่างที่ง่ายมากของการศึกษาที่มีความต้องการในการวัดความแตกต่างพับระหว่างยีนหนึ่งในสองตัวอย่างและหลังจากการฟื้นฟูยีนอ้างอิงเดียว อัตราส่วนแสดงการเปลี่ยนแปลงพับของ GOI ในตัวอย่างที่ 2 เทียบกับตัวอย่างที่ 1 หลังจากแก้ไขยีน Ref เดี่ยว อย่างไรก็ตามมันได้กลายเป็นที่ชัดเจนว่าการเลือกยีนอ้างอิงที่เหมาะสมเพียงครั้งเดียวมักจะเป็นไปไม่ได้และดังนั้นจึงมีการแนะนำวิธีการที่ซับซ้อนมากขึ้นสำหรับการทำให้เป็นปกติ
การทำให้เป็นปกติ
วัตถุประสงค์หลักของการทดลองที่ใช้ PCR ส่วนใหญ่คือการตอบคำถามพื้นฐานว่ามีเป้าหมายอยู่ในตัวอย่างหรือไม่ (ไม่ทราบ UNK) ในระดับที่ง่ายที่สุดนี้ได้รับคำตอบโดยการใช้เจลและตรวจสอบชิ้นส่วนสำหรับการมีหรือไม่มี GOI ที่ต้องการ เมื่อมีชิ้นส่วนอยู่การยืนยันขนาดของชิ้นส่วนจะช่วยให้มั่นใจได้ถึงผลลัพธ์ที่เป็นบวก อย่างไรก็ตามเมื่อไม่อยู่จะมีโอกาสเกิดผลเป็นลบเท็จ ดังนั้นจึงเป็นสิ่งสำคัญที่จะต้องทำการทดสอบซ้ำและทำ PCR เพิ่มเติมอย่างน้อยหนึ่งชุดเพื่อทำหน้าที่เป็นการควบคุม PCR ที่เป็นการโหลดและเป็นบวก สากล, การทดสอบการควบคุมการยับยั้ง, SPUD (ดู การทำให้บริสุทธิ์ตัวอย่างและการประเมินคุณภาพ) สามารถใช้เพื่อสนับสนุนความมั่นใจในผลลบ วิธีการทางเลือกคือการทำการทดสอบที่เฉพาะเจาะจงกับยีนหรือยีนอ้างอิง ตามปกติแล้ว PCR จะวิเคราะห์ยีนอ้างอิง GAPDH, RNA ribosomal RNA 18 ส. หรือ β actin จะทำงานควบคู่ไปกับยีนอ้างอิง GOI และชิ้นส่วนที่เกิดขึ้นจะแสดงเป็นภาพบนเจล GAPDH, RNA ribosomal 18 สและ β แอคทีนเป็นส่วนประกอบและถูกใช้เป็นตัวควบคุมการโหลดในการวิเคราะห์กึ่งเชิงปริมาณ อย่างไรก็ตามในไม่ช้ามันก็เห็นได้ชัดว่ายีนเหล่านี้ไม่ได้แสดงออกอย่างแพร่หลายในความเข้มข้นเดียวกันในเซลล์ทั้งหมดโดยไม่คำนึงถึงการออกแบบการทดลอง ดังนั้นความต้องการที่เกิดขึ้นสำหรับการอ้างอิงที่มั่นคงเมื่อวัตถุประสงค์คือการวัดความเข้มข้นของกรดนิวคลีอิกสัมพัทธ์โดยปกติจะเป็น cDNA แต่ยังเป็น gDNA เมื่อตรวจสอบการเปลี่ยนแปลงจำนวนสำเนาของยีน
Normalization เป็นกระบวนการในการแก้ไขการวัดทางเทคนิคให้เป็นการอ้างอิงที่มีเสถียรภาพเพื่อตรวจสอบความแปรผันทางชีวภาพที่แท้จริง มีหลายวิธีในการทำให้ความแตกต่างทางเทคนิคเป็นปกติซึ่งหมายความว่าต้องเลือกวิธีการที่เหมาะสมสำหรับการทดลองเฉพาะและตรวจสอบ7 เป็นสิ่งสำคัญที่จะต้องตระหนักว่าการนำเทคนิคการทำให้เป็นปกติที่ไม่เหมาะสมมาใช้อาจเป็นอันตรายต่อกระบวนการวิเคราะห์โดยรวมมากกว่าการไม่ทำให้เป็นปกติทั้ง8
ผลกระทบของคุณภาพตัวอย่างในการทำให้เป็นปกติของการวิเคราะห์
ผลของความสมบูรณ์ของตัวอย่างและความบริสุทธิ์ในการวัดปริมาณเป้าหมายโดย qPCR และ RT-qPCR ถูกกล่าวถึงที่ความยาว (การทำให้บริสุทธิ์ตัวอย่างและ การประเมินคุณภาพการควบคุมคุณภาพตัวอย่างและการถอดสคริปต์ย้อนกลับการถอดสคริปต์ย้อนกลับ) แสดงให้เห็นว่าสารยับยั้งในตัวอย่างและการย่อยสลาย RNA มีผลแตกต่างกันในการวัดชิ้นงานที่กำหนด9 สารยับยั้งจะส่งผลต่อการวัดชิ้นงานใดๆแต่เป็นระดับที่แตกต่างกันขึ้นอยู่กับการออกแบบการวิเคราะห์ การย่อยสลายของ RNA ทั้งหมดผลการวัด mRNA และ miRNA10อีกครั้งขึ้นอยู่กับการออกแบบการทดลองโดยรวม ดังนั้นจึงเป็นสิ่งสำคัญที่จะต้องพิจารณาผลกระทบของความเข้มข้นของแม่แบบต่อปฏิกิริยา RT และผลกระทบของคุณภาพของตัวอย่างต่อข้อมูลหลังจากการทำให้เป็นปกติ การทำให้เป็นปกติจะไม่นับผลกระทบของการวิเคราะห์หรือตัวอย่างที่มีคุณภาพต่ำ (ดู การเพิ่มประสิทธิภาพการวิเคราะห์และการตรวจสอบ)
วิธีการฟื้นฟู
ตามหลักการแล้ววิธีการฟื้นฟูจะช่วยลดความผันแปรที่อาจเกิดขึ้นในระหว่างกระบวนการหลายขั้นตอนซึ่งจำเป็นต้องทำการวิเคราะห์ qPCR (รูปที่ 10.6) อย่างไรก็ตามการใช้การทำให้เป็นปกติในขั้นตอนใดขั้นตอนหนึ่งในกระบวนการอาจไม่สามารถควบคุมข้อผิดพลาดทางเทคนิคและ/หรืออคติที่เกิดขึ้นหรือจะถูกนำมาใช้ในระยะก่อนหน้าหรือหลังตามลำดับ วิธีการทำให้เป็นปกติไม่ได้มีความพิเศษร่วมกันดังนั้นการใช้การรวมกันของการควบคุมจึงแนะนำ11

รูปที่ 10 6QPCR เป็นกระบวนการแบบหลายขั้นตอนและแต่ละขั้นตอนจะต้องได้รับการควบคุม การทำให้เป็นปกติต้องได้รับการพิจารณาภายในชุดการควบคุม
วัตถุประสงค์ของการทำให้เป็นปกติคือการให้จุดอ้างอิงที่มีเสถียรภาพซึ่งสามารถอ้างอิงการวัดได้ดังนั้นการเลือกปัจจัยการทำให้เป็นปกติจะต้องเป็นการวัดที่มีความเสถียรตลอดการทดลอง ซึ่งอาจเป็นยีนอ้างอิงที่มีความเสถียรหรือทางเลือกหนึ่งเช่นหมายเลขเซลล์มวลเนื้อเยื่อความเข้มข้น RNA/DNA การขัดขวางภายนอก12หรือการวัดตัวแทนของยีนที่แสดงทั่วโลก
การเลือกยีนอ้างอิง
ยีนอ้างอิงคือเป้าหมายที่ปริมาณไม่เปลี่ยนแปลงอันเป็นผลมาจากการทดลอง เมื่อนับจำนวนการเปลี่ยนแปลงของจำนวนสำเนา DNA ที่จำนวนสำเนาของลำดับความสนใจอาจเปลี่ยนแปลงไปการวัดจะถูกทำให้เป็นมาตรฐานโดยการกำหนดเป้าหมายไปที่ภูมิภาคจีโนมิกอื่นที่ทราบว่าไม่ควรเปลี่ยนแปลง ตัวอย่างของวิธีนี้อาจนำไปใช้คือเมื่อวัดตัวรับปัจจัยการเจริญเติบโตของผิวหนังมนุษย์ 2 (her-3) การขยายจีโนมิก 213 ความไม่เสถียรทางพันธุกรรมของเธอ 2 เป็นตัวบ่งชี้การพยากรณ์โรคในมะเร็งเต้านมและการวัดสถานะการขยายสัญญาณที่แม่นยำของเธอ 2 เป็นสิ่งสำคัญในการจัดการผู้ป่วย สถานะของเธอ 2 สามารถวัดได้โดย qPCR โดยการเปรียบเทียบสำเนาของเธอ 2 กับเป้าหมายจีโนมิกอื่นที่ทำหน้าที่เป็นตัวควบคุม
เมื่อวัดการแสดงออกของยีนยีนอ้างอิงเป็นเป้าหมายที่มีความเข้มข้น mRNA ที่ไม่เปลี่ยนแปลงอันเป็นผลมาจากการทดลอง การศึกษาตัวอย่างจะเป็นการศึกษาที่มีผลต่อการแสดงออกของยีน X ถูกวัดหลังจากการเพิ่มสารประกอบไมโตจีนิกลงในเซลล์โมโนเลเยอร์ จำเป็นต้องมีจุดอ้างอิงเพื่อวัดการเปลี่ยนแปลงของยีน X ดังนั้นยีน (หรือยีน) อื่นที่ทราบว่าไม่ได้รับผลกระทบจาก mitogen ที่เป็นปัญหาก็จะถูกวัดด้วย ซึ่งจะช่วยให้นักวิจัยมีความท้าทายทันทีในการหาเป้าหมาย mRNA ที่ไม่ได้รับผลกระทบจากขั้นตอนการทดลองก่อนที่จะสามารถศึกษา GOI ได้ กระบวนการตรวจสอบยีนอ้างอิงนี้เป็นพื้นฐานสำหรับการวัด GOI ที่แม่นยำ วิธีการที่ใช้กันอย่างแพร่หลายในการทำให้เป็นปกติคือการละเว้นกระบวนการนี้และทำให้ข้อมูลการแสดงออกของยีนเป็นปกติไปยังยีนอ้างอิงที่ยังไม่ได้ตรวจสอบ การปฏิบัตินี้ไม่ได้รับการแนะนำและอยู่ในความขัดแย้งโดยตรงกับแนวทาง MIQE1 การวัดปริมาณของ mRNA โดย RT-qPCR ได้รับผลกระทบจากการเลือกยีนอ้างอิงที่ไม่ถูกต้องเป็นประจำ เป็นที่ยอมรับไม่ได้ที่จะปฏิบัติตามแนวทางปฏิบัติที่ค่อนข้างทั่วไปในการใช้ยีนอ้างอิงเนื่องจากไพรเมอร์อยู่ในตู้แช่แข็งแล้วมันถูกใช้ในอดีตใน blots เหนือมันถูกใช้โดยเพื่อนร่วมงานหรือใช้ในห้องปฏิบัติการอื่นสำหรับการทดลองที่แตกต่างกัน ยีนอ้างอิงต้องได้รับการตรวจสอบภายใต้สถานการณ์การทดลองเฉพาะเพื่อให้มั่นใจว่ายีนอ้างอิงที่เป็นปัญหาจะไม่ได้รับผลกระทบจากการทดลอง หากการตรวจสอบนี้ไม่ได้ดำเนินการและยีนอ้างอิงได้รับผลกระทบจากการทดลองผลลัพธ์อาจไม่ถูกต้องและการตีความที่ตามมามีแนวโน้มที่จะส่งผลให้ข้อมูลที่ไม่มีความหมาย8
มีช่วงของวรรณกรรมทางวิทยาศาสตร์อธิบายวิธีการที่แตกต่างกันสำหรับการฟื้นฟู7-1 4 เช่นเดียวกับจำนวนมากของสิ่งพิมพ์อธิบายโปรโตคอลที่จำเป็นในการระบุยีน Normalizer ที่เหมาะสมที่สุดสำหรับสถานการณ์การทดลองที่กำหนด ในขณะที่ในอดีตคำถามสำคัญคือการเลือกยีนอ้างอิงเดียวหรือหลายตัวการลดต้นทุนการทำงานหมายความว่าแนวทางปฏิบัติที่ดีที่สุดในปัจจุบันได้ย้ายไปสู่การวัดยีนอ้างอิงหลายตัว
การเลือกยีนอ้างอิงที่มีเสถียรภาพจำเป็นต้องให้นักวิเคราะห์ประเมินความเสถียรของ qPCR สำหรับจำนวน (โดยปกติจะ เป็น 10 ถึง 20 ยีน) ของ mRNA ผู้สมัครเป้าหมาย 7 บนชุดย่อยของตัวอย่างที่แสดงถึงการทดสอบและควบคุม mRNA โปรโต คอลเต็มรูปแบบมีอยู่ในภาคผนวก A, โปรโตคอลของคู่มือนี้และอาจใช้ร่วมกับวิธีการวิเคราะห์ที่แตกต่างกันโดยใช้โปรแกรมเช่น REST 15GeNorm14Bestkeeper16หรือ NormFinder17 ขั้นตอนนี้อธิบายโดยละเอียดในส่วนต่อไปนี้การวิเคราะห์ความเสถียรของยีนอ้างอิง
การวิเคราะห์ความเสถียรของยีนอ้างอิง
ยีนอ้างอิงเป็นจุดหมุนสำหรับการวิเคราะห์เชิงปริมาณเชิงสัมพัทธ์ qPCR ดังนั้นจึงเป็นสิ่งสำคัญสำหรับความน่าเชื่อถือของการวิเคราะห์ทั้งหมดที่ยีนอ้างอิงมีเสถียรภาพ ถ้าการแสดงออกของยีนอ้างอิงแตกต่างกันไประหว่างตัวอย่างการเปลี่ยนแปลงจะถูกถ่ายโอนโดยตรงไปยังผลการวัดปริมาณและความแปรปรวนที่เพิ่มขึ้นอาจบดบังผลทางชีวภาพที่สังเกตได้ที่ต้องการหรือยิ่งแย่กว่านั้นอาจสร้างลักษณะเทียมทั้งหมดของผลทางชีวภาพ อันที่ไม่เกี่ยวข้องกับยีนที่น่าสนใจจริงๆ ด้วยเหตุผลเหล่านี้ขอแนะนำอย่างยิ่งให้ปฏิบัติตามมาตรการด้านความปลอดภัยหลายอย่างเพื่อทำให้ความแปรปรวนของยีนอ้างอิงไม่สำคัญและทำการวัดผลกระทบทางชีวภาพที่สำคัญที่สุดเท่าที่จะเป็นไปได้
โดยสรุปแล้วมาตรการความปลอดภัยที่สำคัญที่สุดคือการใช้ยีนอ้างอิงไม่เพียงอย่างเดียวแต่ยังใช้ยีนอ้างอิงอีกสองตัว การแสดงออกของยีนอ้างอิงหลายสามารถเฉลี่ยเพื่อลดความแปรปรวนทางเทคนิคเนื่องจากการปกติ ซึ่งจะเป็นประโยชน์ในการปรับปรุงความสำคัญในการวัดผลกระทบทางชีวภาพขนาดเล็ก อย่างไรก็ตามที่สำคัญกว่านั้นยีนอ้างอิงสองยีนหรือมากกว่านั้นมีการควบคุมร่วมกันเพื่อรักษาเสถียรภาพและการควบคุมสำหรับเหตุการณ์ที่ไม่คาดคิดซึ่งอาจมีผลต่อระดับการแสดงออกของยีนอ้างอิงหนึ่งยีน ด้วยยีนอ้างอิงเดียวอาจมีความเสี่ยงที่อาจตรวจไม่พบอิทธิพลที่ไม่คาดคิดของการแสดงออกของยีนในการวิเคราะห์
อีกหนึ่งมาตรการด้านความปลอดภัยคือการใช้วิธีการมากกว่าหนึ่งวิธีในการระบุยีนอ้างอิงที่มีเสถียรภาพ ต่อไปนี้เป็นตัวอย่างที่แสดงให้เห็นถึงหลายแง่มุมของการฟื้นฟูยีนอ้างอิงรวมถึงประโยชน์ที่เป็นไปได้ในการใช้ทั้งวิธีการ geNorm และ NormalFinder ในชุดข้อมูลเดียวกัน
ตารางที่ 10 3 มีรายการของตัวเลือกยีนอ้างอิงที่ได้รับการประเมินในระหว่างการประชุมเชิงปฏิบัติการที่เราได้ดำเนินการก่อนหน้านี้กับ EMBL ตัวอย่างถูกเก็บรวบรวมจากวัฒนธรรมเซลล์มนุษย์ในกลุ่มการรักษาที่แตกต่างกันสองกลุ่ม ชุดข้อมูลนี้จะถูกใช้เพื่อแสดงให้เห็นถึงแง่มุมของการตรวจสอบยีนอ้างอิง
ทั้งอัลกอริธึม NormFinder และ geNorm ได้รับการพัฒนาขึ้นโดยมีสมมติฐานว่าการทดสอบยีนอ้างอิงจำนวนมากสามารถใช้เพื่อจัดอันดับความเสถียรของตัวเลือกยีนอ้างอิงแต่ละตัว สมมติฐานอาจเป็นจริงได้ตัวอย่างเช่นถ้าตัวเลือกยีนอ้างอิงทั้งหมดแตกต่างกันอย่างต่อเนื่องรอบระดับการแสดงออกที่เสถียร อย่างไรก็ตามสิ่งนี้อาจไม่จำเป็นต้องเป็นความจริงเสมอไป เพื่อหลีกเลี่ยงผลลัพธ์ที่ทำให้เข้าใจผิดจึงเป็นเรื่องที่รอบคอบในการหลีกเลี่ยงการควบคุมและโดยเฉพาะอย่างยิ่งผู้ที่มียีนอ้างอิงที่ควบคุมร่วมกัน
รายการตัวเลือกยีนอ้างอิงที่แสดงใน ตารางที่ 10 3 ได้รับเลือกโดยเฉพาะให้เลือกยีนที่อยู่ในคลาสการทำงานที่แตกต่างกันลดโอกาสที่ยีนอาจถูกควบคุมร่วมกัน ข้อยกเว้นที่โดดเด่นคือ GAPDH ซึ่งมีอยู่ที่นี่ในสองรุ่น แม้ว่าสิ่งนี้จะไม่ส่งผลกระทบต่อการวิเคราะห์นี้แต่วิธีปฏิบัติที่ดีที่สุดคือหลีกเลี่ยงการป้อนยีนหลายรายการที่อาจสงสัยว่าเป็นการควบคุมร่วมกัน
อัลกอริธึมแรกที่แสดงคือ geNorm ซึ่งจะให้การประเมินความสามารถของยีนโดยการคำนวณการวัดความเสถียรของยีนที่เรียกว่าค่า M ซึ่งขึ้นอยู่กับการเปรียบเทียบคู่ระหว่างตัวเลือกยีนอ้างอิงที่วิเคราะห์และตัวเลือกยีนอ้างอิงอื่นๆทั้งหมดในชุดข้อมูล มันจะดำเนินการในลักษณะซ้ำซึ่งหมายความว่าในตัวอย่างนี้ขั้นตอนจะดำเนินการครั้งแรกกับผู้สมัครยีนอ้างอิงทั้งหมด 15 คนที่มีเสถียรภาพน้อยที่สุดจะถูกลบออกกระบวนการจะทำซ้ำใน 14 ที่เหลือผู้สมัครที่มีเสถียรภาพน้อยที่สุดที่สองจะถูกลบออก และอื่นๆจนกว่ายีนอ้างอิงสองตัวจะยังคงอยู่
อาจมีบางครั้งที่การระบุยีนอ้างอิงที่เสถียรที่สุดอาจเป็นเรื่องที่ท้าทายเป็นพิเศษ กรณีหนึ่งอาจเป็นเมื่อผู้สมัครยีนอ้างอิงทั้งหมดทำงานได้ไม่ดี อีกกรณีหนึ่งอาจเป็นถ้าผู้สมัครยีนอ้างอิงทั้งหมดทำงานได้ดี ในการแยกความแตกต่างระหว่างสองกรณีนี้แนวทางที่เป็นประโยชน์คือการอ้างอิงยีนที่มีค่า M ต่ำกว่า 0.5 อาจถือว่าแสดงได้อย่างเสถียร
อัลกอริทึมที่สองที่จะแสดงคือ NormalFinder ซึ่งเป็นแพคเกจการวิเคราะห์ยีนอ้างอิงที่มีอยู่อย่างอิสระ (ภาคผนวก B, แหล่งข้อมูลเพิ่มเติม) อัลกอริทึมที่อยู่เบื้องหลังใช้วิธีการแบบ ANOVA เพื่ออ้างอิงการประเมินความเสถียรของยีนในการที่ทั้งกลุ่มและกลุ่มย่อยจะถูกวิเคราะห์เพื่อหาความแปรปรวน ข้อดีอย่างหนึ่งของเรื่องนี้คือมาตรการที่ได้มานั้นเกี่ยวข้องโดยตรงกับระดับการแสดงออกของยีน ดังนั้นค่าเบี่ยงเบนมาตรฐานของ 0.20 ในหน่วย Cq จึงแสดงถึงความแปรผันประมาณ 15% ในระดับนิพจน์หมายเลขสำเนาของตัวเลือกยีนอ้างอิงเฉพาะ
เพื่อความสะดวกในการสาธิตนี้คุณสามารถเข้าใช้งานแพคเกจการวิเคราะห์ทั้งสองนี้ได้โดยใช้ซอฟต์แวร์การวิเคราะห์ข้อมูล Genex (multid) แต่ยังสามารถใช้เป็นแพคเกจอิสระ (ภาคผนวก B, แหล่งข้อมูลเพิ่มเติม)
แผนภูมิแท่งที่แสดงใน รูปที่ 10 7 แสดงให้เห็นถึงยีนอ้างอิงที่จัดอันดับตามมาตรการความเสถียรที่เกี่ยวข้องโดยใช้อัลกอริทึมทั้งสอง นอกจากนี้กราฟที่แสดงค่าเบี่ยงเบนมาตรฐานสะสมจาก NormalFinder ยังระบุว่าการรวมกันของยีนอ้างอิงที่ดีที่สุดสามยีนอาจทำให้เกิดการปรับปรุงความเสถียรได้

รูปที่ 10 7แผนภูมิแท่งแสดงการวัดความเสถียร: ค่า M สำหรับ geNorm และค่าเบี่ยงเบนมาตรฐานสำหรับ NormalFinder นอกจากนี้กราฟที่แสดงค่าเบี่ยงเบนมาตรฐานสะสมจาก NormalFinder ยังระบุว่าการรวมกันของยีนอ้างอิงที่ดีที่สุดสามยีนอาจทำให้เกิดการปรับปรุงความเสถียรได้ ชุดข้อมูลถูกสร้างขึ้นจากการวิเคราะห์ที่ออกแบบมาสำหรับตัวเลือกยีนอ้างอิงที่แสดงในตารางที่ 10.3 และวัดจากการเพาะเซลล์มนุษย์ในกลุ่มการรักษาที่แตกต่างกันสองกลุ่ม สังเกตว่าในกรณีนี้อัลกอริธึมความเสถียรของยีนอ้างอิง geNorm และ NormalFinder ไม่เห็นด้วยกับยีนอ้างอิงที่ดีที่สุด

รูปที่ 10 8โปรไฟล์การแสดงออกที่เป็นศูนย์กลางของตัวเลือกยีนอ้างอิงของสองตัวอย่างในแต่ละกลุ่มการรักษา ตัวอย่างที่ 1 และ 2 อยู่ในกลุ่มการรักษาแรกและตัวอย่างที่ 3 และ 4 อยู่ในกลุ่มการรักษาที่สอง โปรไฟล์นิพจน์ของ SDHA และ CanX จะแสดงเป็นสีแดง โปรไฟล์นิพจน์ของ UBC จะแสดงเป็นสีเหลือง ตารางจะแสดงรายการค่า Cq ที่วัดได้ในชุดข้อมูล
เนื่องจากโปรไฟล์การแสดงออกเบี่ยงเบนจึงเป็นไปได้ว่า SDHA และ CanX ถูกควบคุมโดยทางเลือกในการรักษาที่แตกต่างกันและดังนั้นจึงไม่เหมาะกับยีนอ้างอิง ลบเหล่านี้ออกจากชุดข้อมูลและทำซ้ำผลการวิเคราะห์ในข้อตกลงระหว่างทั้งสองอัลกอริทึมและทางเลือกที่ดีที่สุดของยีนอ้างอิงคือ EIF4A2 และ ATP53 (รูปที่ 10.9) ในการคำนวณ NormaFinder ของการเบี่ยงเบนมาตรฐานสะสมก็ยังเห็นได้ชัดว่าการเพิ่มยีนอ้างอิงมากขึ้นไม่ได้ปรับปรุงเสถียรภาพ

รูปที่ 10 9การตรวจสอบโปรไฟล์การแสดงออกและค่า Cq ที่วัดได้ (รูปที่ 10 8) แสดงความกังวลว่า SDHA และ CanX อาจถูกควบคุมร่วมกันในการวิเคราะห์ที่ใช้ การควบคุมร่วมอาจรบกวนอัลกอริธึมความเสถียรของยีนอ้างอิง แผนภูมิแท่งแสดงการวัดความเสถียร: a) ค่า M สำหรับ geNorm และ B) ส่วนเบี่ยงเบนมาตรฐานสำหรับ NormalFinder ชุดข้อมูลจะเหมือนกับชุดข้อมูลที่ใช้ในรูปที่ 10.8 ยกเว้นว่าข้อมูลสำหรับ SDHA และ CanX ถูกลบออกแล้ว สังเกตว่าด้วยข้อมูลที่ลดลงนี้ตั้งค่าอัลกอริธึมความเสถียรของยีนอ้างอิง geNorm และ NormalFinder เห็นด้วยกับยีนอ้างอิงที่ดีที่สุด
การวิเคราะห์ข้อมูลในตัวอย่างนี้ทำหน้าที่แสดงให้เห็นว่าการใช้ geNorm และ NormFinder แบบขนานช่วยให้สามารถระบุตัวตนของผู้สมัครยีนอ้างอิงที่ควบคุมร่วมกันและการลบยีนเหล่านี้ออกจากการศึกษาต่อไปจะให้การระบุยีนอ้างอิงขั้นสุดท้ายที่สามารถนำมาใช้ได้อย่างมั่นใจมากกว่าหลังจากใช้ การวิเคราะห์เพียงครั้งเดียว การระบุและการเลือกยีนอ้างอิงที่มีเสถียรภาพนำไปสู่ความปลอดภัยที่มากขึ้นของการวิเคราะห์ข้อมูล
วิธีการ Normalization ทางเลือก
ในขณะที่ normalization เพื่ออ้างอิงยีนเป็นวิธีที่พบมากที่สุดสำหรับการวิเคราะห์ normalization มีสถานการณ์ที่วิธีการนี้ไม่เหมาะสมเช่นเมื่อจำนวนมากของยีนในกลุ่มที่แตกต่างกันของตัวอย่างจะถูกเปรียบเทียบหรือเมื่อ profiling miRNA ในสถานการณ์เหล่านี้จำเป็นต้องนำกลยุทธ์ทางเลือกมาใช้
การฟื้นฟูมวลเนื้อเยื่อหรือหมายเลขเซลล์
การวัดจำนวนเซลล์หรือมวลเนื้อเยื่อที่จะใช้เป็นปัจจัยการทำให้เป็นปกติไม่ใช่เรื่องง่ายอย่างที่อาจปรากฏขึ้นเป็นครั้งแรก การทดลองเพาะเลี้ยงเซลล์นั้นค่อนข้างง่ายที่จะทำให้เป็นปกติตามการนับเซลล์ อย่างไรก็ตามการเพิ่มการรักษาอาจส่งผลกระทบต่อสัณฐานวิทยาของเซลล์ทำให้อัตราส่วนของจำนวนเซลล์ต่ออาร์เอ็นเอ/ยีนทั้งหมดที่แสดงเมื่อเทียบกับวัฒนธรรมการควบคุม การทดลองอาจส่งผลให้เกิดการผลิตเมทริกซ์เซลล์พิเศษทำให้เกิดความแตกต่างในประสิทธิภาพการสกัดกรดนิวคลีอิก
เนื้อเยื่อทางชีวภาพอาจมีความแตกต่างกันอย่างมากภายในและระหว่างวัตถุโดยมีความแตกต่างมากขึ้นเมื่อเปรียบเทียบกับเนื้อเยื่อที่เป็นโรค แม้เนื้อเยื่อที่ซับซ้อนน้อยเช่นเลือดอาจแตกต่างกันอย่างมากในการนับเซลล์และองค์ประกอบเช่นการแสดงออกของยีนแตกต่างกันอย่างมากระหว่างผู้บริจาคที่มีสุขภาพดีอย่างเห็นได้ชัด18
ความล่าช้าในกระบวนการที่ใช้ในการทำให้กรดนิวคลีอิกบริสุทธิ์จะส่งผลให้เกิดการเปลี่ยนแปลงใน RNA ที่วัดได้ ตัวอย่างเช่นความล่าช้าในการประมวลผลเซลล์ mononuclear ในเลือดส่วนปลายและการแยก RNA ออกจากเซลล์ส่งผลให้เกิดการเปลี่ยนแปลงอย่างมากในการแสดงออกของยีน19 วิธีการที่อยู่ภายใต้ขั้นตอนการสกัดยังเป็นแหล่งที่มาหลักของความแปรผันทางเทคนิค แม้แต่กระบวนการแยกที่เลือกไว้สำหรับการสุ่มตัวอย่างเซลล์ที่ได้มาจากเลือดและการทำให้บริสุทธิ์ RNA ทำให้เกิดความแตกต่างในโปรไฟล์การแสดงออกของยีนที่ชัดเจน 20 ดังนั้นการพิจารณาการทำให้เป็นปกติครั้งแรกคือเพื่อให้แน่ใจว่าการเก็บรวบรวมและการประมวลผลนั้นเหมือนกันอย่างแน่นอนสำหรับตัวอย่างทั้งหมด จากนั้นจึงเป็นสิ่งสำคัญที่จะต้องดำเนินการควบคุมคุณภาพอย่างเพียงพอเพื่อให้มั่นใจในความเข้มข้นความสมบูรณ์และความบริสุทธิ์ของตัวอย่าง (การทำให้บริสุทธิ์ตัวอย่างและ การประเมินคุณภาพ tand โปรโตคอลที่เกี่ยวข้องใน ภาคผนวกA)
การฟื้นฟูความเข้มข้นของ RNA
อย่างน้อยที่สุดการประมาณความเข้มข้นของแม่แบบ (DNA สำหรับ qPCR หรือ RNA สำหรับ RT-qPCR) เป็นสิ่งสำคัญและตามที่กล่าวไว้ใน การทำให้บริสุทธิ์ตัวอย่างและการประเมินคุณภาพจำเป็นอย่างยิ่งที่จะต้องตรวจสอบให้แน่ใจว่าเครื่องมือเดียวกันนี้ใช้สำหรับการวัดทั้งหมดเนื่องจากการกำหนดความเข้มข้นของกรดนิวคลีอิกนั้นขึ้นอยู่กับตัวแปรและเทคนิค
เมื่อวัดความเข้มข้นรวมของ RNA ตัวอย่างส่วนใหญ่จะประกอบด้วย rRNA โดยมีเพียงส่วนเล็กๆที่ประกอบด้วย mRNA ที่น่าสนใจเมื่อตรวจสอบการแสดงออกของยีนหรือ sncRNA เมื่อตรวจสอบการควบคุมการแสดงออกของยีน ซึ่งหมายความว่าถ้าความเข้มข้น rRNA เพิ่มขึ้นเล็กน้อยแต่ mRNA ยังคงคงที่ความเข้มข้น RNA ทั้งหมดจะเพิ่มขึ้น ความเข้มข้นของ mRNA ต้องเพิ่มขึ้นอย่างมากเพื่อทำให้ความเข้มข้นของ RNA ทั้งหมดเพิ่มขึ้นอย่างเห็นได้ชัด ดังนั้นความเข้มข้น rRNA จึงเป็นการวัดความเข้มข้นของ mRNA ที่ไม่น่าเชื่อถือแต่สำหรับโปรโตคอลจำนวนมากจำเป็นต้องมีความเข้มข้นของ RNA เท่ากันเพื่อให้แน่ใจว่า การถอดสคริปต์ย้อนกลับถูกต้อง (ดูการถอดสคริปต์ย้อนกลับ)
การฟื้นฟูการแสดงออกของยีนทั่วโลก
เมื่อวัดเป้าหมายจำนวนมากนักวิเคราะห์สามารถประมาณค่าเฉลี่ยทั่วโลกของการแสดงออกของยีนทั้งหมดและระบุลำดับ RNA ที่ควบคุมซึ่งเบี่ยงเบนไปจากค่าเฉลี่ยนี้ วิธีการนี้โดยทั่วไปจะใช้สำหรับการทำให้อาร์เรย์การแสดงออกของยีนเป็นปกติ มันเป็นทางเลือกที่มีค่าในการใช้ยีนอ้างอิงและอาจจะดีกว่าที่เป้าหมายจำนวนมากจะถูกวัด.
อีกวิธีหนึ่งที่เพิ่งได้รับการสำรวจคือการวัดองค์ประกอบที่เกิดซ้ำที่แสดงออกมาจากภายนอก (ERE) ที่มีอยู่ภายใน mRNA หลายตัว หลายสายพันธุ์มีองค์ประกอบที่ทำซ้ำเหล่านี้ (ALU ในไพรเมต, องค์ประกอบ B ในหนู) ซึ่งสามารถให้การประมาณค่าของเศษส่วน mRNA การวัดลำดับเป้าหมายเหล่านี้ได้รับการแสดงให้เห็นว่าเป็นระบบ normalizing ทั่วไป9 (Le Bert, et al., ในการเตรียมการ) และอาจเสนอโซลูชันสากลหรือทางเลือกสำหรับการทดลองที่ซับซ้อนซึ่งการรวมยีนอ้างอิงที่มีเสถียรภาพไม่สามารถใช้งานได้
การทำให้ข้อมูล miRNA เป็นปกติ
ยังไม่มีรายงานของยีนอ้างอิงสากล miRNA ดังนั้นการเลือกระบบการทำให้เป็นปกติจึงยังคงเป็นเชิงประจักษ์ หากเป็นไปได้อาจมีการระบุ miRNA ที่มีความคงตัวคงที่จากวิธีการแบบทั่วทั้งจีโนมเช่นไมโครอาร์เรย์ นอกจากนี้ยังมีการใช้ Nucleolar RNAs (snoRNAs) ขนาดเล็กเป็นยีนอ้างอิง การแสดงออกของยีนทั่วโลกยังเป็นวิธีที่มีประโยชน์ในการทำให้นิพจน์ miRNA เป็นปกติเมื่อไม่ทราบการอ้างอิงที่เสถียรและมีการวิเคราะห์เป้าหมายหลายร้อยเป้าหมาย21,22,23 วิธีนี้เหมาะสมกว่าสำหรับผู้ที่ใช้วิธีการที่ส่งผลให้ได้รับ miRNA ทั้งหมดเป็น cDNA ในรูปแบบมัลติเพล็กเช่นระบบ Exiqon และ miQPCR (โปรดดู Castoldi et al. ใน PCR Technologies นวัตกรรมปัจจุบัน24)
การทำซ้ำทางชีวภาพและทางเทคนิค
The purpose of normalization is to avoid systematic errors and to reduce data variability for the eventual statistical analysis. อีกแง่มุมที่สำคัญของการตั้งค่าข้อมูลสำหรับการวิเคราะห์ทางสถิติคือการใช้การทำซ้ำข้อมูล
การทำซ้ำทางชีวภาพเป็นสิ่งจำเป็นอย่างยิ่งสำหรับการวิเคราะห์ทางสถิติ ระดับนัยสำคัญทางสถิติมักถูกตั้งค่าไว้ที่จุดตัดนัยสำคัญ 5 เปอร์เซ็นต์ สำหรับผลกระทบทางชีวภาพที่ใกล้เคียงกับระดับนัยสำคัญดังกล่าวอาจจำเป็นต้องมีการทำซ้ำทางชีวภาพอย่างน้อย 20 ครั้งเพื่อกำหนดระดับนัยสำคัญของการวิเคราะห์ (1:20 สอดคล้องกับ 5%) ในความเป็นจริงมีการแนะนำว่าอย่างน้อย 50 เท่าของจำนวนการสังเกตที่จะต้องบันทึกสำหรับการประมาณที่ถูกต้องของความสำคัญ25เช่นในลำดับของพันตัวอย่างทางชีวภาพ โดยธรรมชาติแล้วข้อจำกัดในทางปฏิบัติมักจะไม่อนุญาตให้มีการทำซ้ำทางชีวภาพในระดับเหล่านี้ นอกจากนี้การประมาณการที่แม่นยำของจำนวนของการทำซ้ำทางชีวภาพที่จำเป็นเพื่อให้เป็นไปตามระดับนัยสำคัญที่กำหนดยังขึ้นอยู่กับระดับของความแปรปรวนของข้อมูล อย่างไรก็ตามสิ่งสำคัญคือต้องตระหนักว่าข้อผิดพลาดทั่วไปคือการประเมินจำนวนที่จำเป็นของการทำซ้ำทางชีวภาพต่ำเกินไปเพื่อให้ได้ข้อสรุปที่เชื่อถือได้ ขอแนะนำให้ทำการศึกษานำร่องเบื้องต้นเพื่อประเมินความแปรปรวนโดยธรรมชาติของการทดสอบและขนาดที่เป็นไปได้ของผลกระทบทางชีวภาพที่สังเกตได้เพื่อให้มีพื้นฐานที่ดีในการประมาณจำนวนที่จำเป็นของการทำซ้ำทางชีวภาพ26
การทำซ้ำทางเทคนิคจะไม่ถูกนำมาใช้โดยตรงสำหรับการวิเคราะห์ทางสถิติ แต่จะใช้การทำซ้ำทางเทคนิคในการสำรองตัวอย่าง (ในกรณีที่ตัวอย่างบางตัวอย่างสูญหายในกระบวนการจัดการทางเทคนิค) และเพื่อปรับปรุงการประเมินความถูกต้องของข้อมูล การทำซ้ำทางเทคนิคสามารถปรับปรุงความถูกต้องของข้อมูลได้หากสมมติฐานนั้นเป็นจริงว่าการทำซ้ำนั้นมีความแตกต่างกันอย่างมากในเรื่องการวัดที่แม่นยำในแต่ละขั้นตอนของกระบวนการจัดการทางเทคนิค ค่าเฉลี่ยของการทำซ้ำทางเทคนิคจะใกล้เคียงกับการวัดที่แม่นยำมากขึ้น ผลของการทำซ้ำทางเทคนิคโดยเฉลี่ยสามารถแสดงได้โดยสังเกตขนาดของช่วงความเชื่อมั่นในชุดข้อมูลจำลองที่มีความผันแปรที่กำหนดไว้ล่วงหน้าเช่นค่าเบี่ยงเบนมาตรฐานที่ตั้งไว้ที่หนึ่ง ดังที่เห็นใน ตารางที่ 10.4ช่วงความเชื่อมั่นจะน้อยลงโดยมีจำนวนการทำซ้ำทางเทคนิคที่เพิ่มขึ้น (ตัวอย่าง) ซึ่งแสดงให้เห็นถึงการประมาณการที่แม่นยำยิ่งขึ้นของการวัดที่แม่นยำ ยิ่งไปกว่านั้นการลดช่วงความเชื่อมั่นนั้นเป็นเรื่องที่น่าทึ่งมากที่สุดเมื่อมีการทำซ้ำทางเทคนิคจำนวนน้อย การเพิ่มจำนวนสำเนาจาก 2 – 3 จะลดช่วงความเชื่อมั่นจาก 8.99 – 2.48 นั่นคือการปรับปรุงความแม่นยำมากกว่า 3 เท่าในการประเมินการวัดที่แม่นยำ ในขณะที่การทำซ้ำเพิ่มเติมยังคงปรับปรุงการประมาณความแม่นยำของการวัดผลจะลดลง ดังนั้นจึงเห็นได้ชัดว่าในกรณีที่ความแปรปรวนในการจัดการทางเทคนิคเป็นปัญหาอาจเป็นประโยชน์อย่างมากที่จะใช้สามเท่าแทนที่จะใช้ซ้ำกัน
การทำซ้ำทางเทคนิคสามารถเก็บได้หลายขั้นตอนตลอดกระบวนการจัดการตัวอย่างรวมถึงการแยก RNA การถอดสคริปต์ย้อนกลับและการตรวจจับ QPCR ถ้าตรวจพบการทำซ้ำทางเทคนิคในหลายขั้นตอนการออกแบบการทดลองที่ซ้อนกันจะถูกสร้างขึ้น การศึกษานำร่องที่ใช้ประโยชน์จากการออกแบบทดลองที่ซ้อนกันอาจช่วยในการระบุขั้นตอนการจัดการตัวอย่างที่มีส่วนช่วยในการจัดการทางเทคนิคมากที่สุดและแผนการสุ่มตัวอย่างที่ดีที่สุดสามารถคำนวณได้ตามข้อมูลนี้27
การวิเคราะห์ทางสถิติและการแสดงข้อมูล
การวิเคราะห์ทางวิทยาศาสตร์ของศูนย์ข้อมูลทางชีวภาพเกี่ยวกับการกำหนดและการทดสอบสมมติฐาน การกำหนดสมมติฐานต้องมีความเข้าใจอย่างละเอียดเกี่ยวกับเงื่อนไขและตัวแปรของการวิเคราะห์ การทดสอบสมมติฐานที่ประสบความสำเร็จเกี่ยวข้องกับการดำเนินการอย่างรอบคอบและการออกแบบการทดลองที่เหมาะสมเพื่อเพิ่มสัญญาณที่สามารถสังเกตได้ที่ต้องการในขณะที่ลดความแปรปรวนทางเทคนิค ในบริบทนี้จะเป็นประโยชน์ในการแยกแยะระหว่างการศึกษาเชิงสำรวจและเชิงยืนยัน (รูปที่ 10.10)

รูปที่ 10 10ผังงานแสดงการดำเนินการที่เกี่ยวข้องในการวิเคราะห์ทางสถิติเชิงสำรวจและเชิงยืนยัน ด้านซ้ายของรูปก่อนลูกศรประแสดงการดำเนินการในการศึกษาทางสถิติเชิงสำรวจ ด้านขวามือของรูปหลังจากลูกศรประแสดงการดำเนินการในการศึกษาทางสถิติยืนยัน
วัตถุประสงค์ของการศึกษาเชิงสำรวจคือการวิเคราะห์ข้อมูลด้วยเทคนิคที่แตกต่างกันหนึ่งหรือหลายอย่างเพื่อยืนยันสมมติฐาน ชุดข้อมูลอาจถูกกำหนดใหม่และ/หรือเทคนิคการวิเคราะห์ที่แตกต่างกันอาจถูกนำมาใช้ซ้ำเพื่อสนับสนุนสมมติฐานหนึ่งหรือหลายอย่าง การศึกษาเชิงสำรวจจึงมีความยืดหยุ่นอย่างมากต่อรายละเอียดของคำถามทางวิทยาศาสตร์ใดๆ อย่างไรก็ตามการตรวจสอบการทดสอบสมมติฐานในชุดข้อมูลชุดหนึ่งซ้ำอาจนำไปสู่ปัญหาที่ทำลายข้อสรุปทางสถิติ นี่เป็นเพราะการทดสอบหลายครั้ง, ซึ่งหมายถึงความจริงที่ว่าการทดสอบทางสถิติที่มีสมมติฐานอิสระหลายอย่างมีแนวโน้มที่จะให้ความสำคัญในเชิงบวกและโอกาสของการเพิ่มขึ้นนี้เป็นสมมติฐานเพิ่มเติมมีการทดสอบ, แม้ว่าการแจกแจงความน่าจะเป็นพื้นฐานจะเหมือนกัน. เพื่อหลีกเลี่ยงผลทางสถิติที่ทำให้เข้าใจผิดการศึกษาเชิงสำรวจจึงมักรวมกับการศึกษายืนยัน
ข้อกำหนดสำหรับการศึกษายืนยันนั้นขึ้นอยู่กับเกณฑ์ทางสถิติที่เข้มงวดกว่า ประการแรกสมมติฐานของการศึกษารวมถึงเกณฑ์สำหรับความสำคัญจะต้องได้รับการกำหนดก่อนการเก็บรวบรวมข้อมูลและก่อนการวิเคราะห์ นอกจากนี้ชุดข้อมูลสำหรับการวิเคราะห์ยังจำเป็นต้องได้รับการเก็บรวบรวมเพื่อวัตถุประสงค์นี้โดยเฉพาะ การนำชุดข้อมูลจากการศึกษาเชิงสำรวจมาใช้ใหม่ในการศึกษาเชิงยืนยันไม่ถูกต้องตามสถิติเนื่องจากชุดข้อมูลนั้นจะสนับสนุนสมมติฐานที่เสนอโดยเนื้อแท้ ผลลัพธ์สุดท้ายของการศึกษายืนยันคือสมมติฐานที่ถูกปฏิเสธหรือยอมรับตามเกณฑ์ที่ระบุไว้ล่วงหน้า
Statistical Tests
สำหรับการทดสอบทางสถิติความเป็นไปได้ที่ปรากฏการณ์ที่สังเกตได้จะถูกวิเคราะห์โดยบังเอิญ นี่เรียกว่าสมมุติฐานว่าง28 ถ้าปรากฏการณ์ที่สังเกตพบหายากตามสมมติฐานว่างข้อสรุปก็คือไม่น่าเป็นไปได้ที่สมมติฐานว่างจะถูกต้อง สมมติฐานว่างจะถูกปฏิเสธและยอมรับความเป็นไปได้ของสมมติฐานทางเลือกว่ามีนัยสำคัญ
ความเป็นไปได้โดยประมาณที่ปรากฏการณ์ที่สังเกตได้เกิดขึ้นจากการสุ่มโอกาสเรียกว่า ค่า EP TH EP- ค่าจะถูกวัดในช่วงตั้งแต่ 0 ถึง 1 หรือเทียบเท่าในหน่วยเปอร์เซ็นต์ เกณฑ์ทางสถิติสำหรับการศึกษายืนยันประกอบด้วยการตัดอัลฟาซึ่งคำนวณ ค่า DP จะแสดงถึงความสำคัญของปรากฏการณ์ที่สังเกต โดยทั่วไปจะใช้การตัดอัลฟาที่ร้อยละ 5 แม้ว่าจะต้องปรับให้เหมาะสมกับเกณฑ์ที่ต้องการและจำเป็นที่เฉพาะเจาะจงสำหรับเรื่องของการศึกษา
อัลกอริธึมจำนวนมากได้รับการพัฒนาขึ้นสำหรับ calculatin GP- ค่าภายใต้สมมติฐานต่างๆและเพื่อวัตถุประสงค์ที่แตกต่างกัน อัลกอริทึมทั่วไปคือการทดสอบ T ของนักเรียน การทดสอบ T ของนักเรียนจะใช้ในการคำนวณ ค่า AP โดยยึดตามความแตกต่างของค่าเฉลี่ยระหว่างข้อมูลสองกลุ่ม สมมติฐานหลักของการทดสอบ T ของนักเรียนคือข้อมูลทั้งสองกลุ่มนั้นเป็นอิสระและสอดคล้องกับการแจกแจงปกติ ข้อดีของการทดสอบ T ของนักเรียนคือมันมีประสิทธิภาพเมื่อเทียบกับการทดสอบทางสถิติแบบไม่ใช้พารามิเตอร์29 การทดสอบแบบไม่ใช้พาราเมตริกที่เทียบเท่ากับการทดสอบ T ของนักเรียนอาจเป็นหนึ่งในการทดสอบทางสถิติที่ไม่ใช้พาราเมตริกที่รู้จักกันดีที่สุดการทดสอบอันดับของ Wilcoxon (บางครั้งเรียกว่าการทดสอบ Mann-Whitney U ไม่ควรสับสนกับการทดสอบอันดับที่มีเครื่องหมาย Wilcoxon ซึ่งใช้ในการเปรียบเทียบสองกลุ่มที่จับคู่) การทดสอบทางสถิติที่ไม่ใช่พาราเมตริกเช่นการทดสอบ wilcoxon ranksum มีข้อได้เปรียบเหนือการทดสอบทางสถิติแบบพาราเมตริกเช่นการทดสอบ t ของนักเรียนซึ่งไม่ได้ขึ้นอยู่กับสมมติฐานก่อนหน้าของการแจกแจงชุดข้อมูล การทดสอบของ Kolmogorov- Smirnov สำหรับการกระจายตัวตามปกติอาจใช้ในการตัดสินใจว่าจะใช้การทดสอบ T ของนักเรียนหรือหนึ่งในการทดสอบแบบไม่ใช้พารามิเตอร์
นอกจากตัวเลือกของอัลกอริธึมสำหรับ การคำนวณ Rp - value แล้วชุดข้อมูลที่ป้อนเข้าสู่ อัลกอริธึมการคำนวณ EP - value อาจถูกจัดการเพื่อช่วยในการตรวจสอบคุณสมบัติที่ต้องการในชุดข้อมูล การรวมกันของขั้นตอนการจัดการข้อมูลดิบและ อัลกอริธึมการคำนวณตัวเลือก FP - ค่าเป็นส่วนหนึ่งของการสร้างแบบจำลองสมมติฐาน
มีเสรีภาพในการสร้างแบบจำลองสมมติฐานในขั้นตอนการสำรวจของการวิเคราะห์ทางสถิติและนี่เป็นส่วนสำคัญของการสอบถามทางวิทยาศาสตร์ อย่างไรก็ตามสมมติฐานไม่เคยได้รับการพิสูจน์โดยใช้วิธีการทางวิทยาศาสตร์และสถิติ วิธีการทางวิทยาศาสตร์ที่ถูกต้องคือการกำหนดสมมติฐานว่างใช้ชุดข้อมูลที่เป็นอิสระ (โดยเฉพาะชุดข้อมูลที่รวบรวมใหม่) และยอมรับหรือปฏิเสธสมมติฐานว่างตามผังงานการศึกษายืนยัน (รูปที่ 10.10)
เทคนิคการสร้างภาพสำหรับการวิเคราะห์แบบสม่ำเสมอ
เช่นเดียวกับวิธีการวิเคราะห์ที่มีอยู่มากมายก็ยังมีเทคนิคการแสดงภาพข้อมูลมากมายให้เลือก สำหรับการวิเคราะห์ข้อมูลแบบรวมเป็นหนึ่งเดียวกันแผนภูมิแท่งแบบง่ายที่มีแถบค่าคลาดเคลื่อนที่สัมพันธ์กันเป็นเทคนิคการแสดงภาพที่เหมาะสม แม้ว่านี่จะเป็นเทคนิคการแสดงภาพทั่วไปและเรียบง่ายแต่ก็มีปัญหาที่ควรเน้น ประการแรกแถบค่าคลาดเคลื่อนอาจแสดงให้เห็นถึงแหล่งที่มาที่แตกต่างกันของความแปรปรวนโดยธรรมชาติของข้อมูล (ค่าเบี่ยงเบนมาตรฐาน, SD) หรือความเที่ยงตรงที่มีการกำหนดค่าเฉลี่ย ประการที่สองความแม่นยำที่ค่าเฉลี่ยได้รับการกำหนดสามารถแสดงได้ในรูปแบบต่างๆ แต่ในที่สุดก็ขึ้นอยู่กับการรวมกันของความแปรปรวนโดยธรรมชาติของข้อมูลพร้อมกับจำนวนตัวอย่าง (N) และในรูปแบบดิบของมันเรียกว่าข้อผิดพลาดมาตรฐานของค่าเฉลี่ย (SEM, สมการ 1):

สมการ 1SEM
อย่างไรก็ตาม SEM ไม่ได้เป็นมาตรการที่ใช้งานง่ายมากและไม่ตรงไปข้างหน้าเพื่อเปรียบเทียบ SEM จากการทดลองที่แตกต่างกันในทางที่มีความหมาย วิธีที่นิยมมากขึ้นในการแสดงให้เห็นถึงความแม่นยำของค่าเฉลี่ยโดยประมาณและการระบุความสำคัญทางสถิติในแบบกราฟิกคือช่วงความเชื่อมั่น (CI, สมการ 2):

สมการ 10 2CL
การปรากฏตัวของ SEM สามารถรับรู้ได้ในสมการสำหรับช่วงความเชื่อมั่นเป็นอัตราส่วนระหว่างค่าเบี่ยงเบนมาตรฐาน (SD) และรากที่สองของจำนวนตัวอย่าง (N) และทำให้เห็นได้ชัดว่าช่วงความเชื่อมั่นจะขึ้นอยู่กับ SEM ขีดจำกัดล่างของช่วงความเชื่อมั่นจะถูกสร้างขึ้นโดยการลบ SEM คูณด้วยเปอร์เซ็นต์ไทล์ของการแจกแจงแบบ t จากค่าเฉลี่ย ขีดจำกัดบนของช่วงความเชื่อมั่นจะถูกสร้างขึ้นโดยการเพิ่ม SEM คูณด้วยเปอร์เซ็นต์ไทล์ของการแจกแจงแบบ t จากค่าเฉลี่ย ระดับความเชื่อมั่นของช่วงความเชื่อมั่นจะถูกกำหนดโดยระดับความเชื่อมั่นที่สัมพันธ์กับค่าวิกฤต t* ซึ่งโดยปกติจะเป็นระดับความเชื่อมั่น 95%
รูปที่ 10.1 1 แสดงกราฟแท่งที่มีแถบข้อผิดพลาดแสดงช่วงความเชื่อมั่นร้อยละ 95 ภายในกลุ่มทดลองแต่ละกลุ่มโดยเน้นความไม่แน่นอนที่เกี่ยวข้องกับการประมาณค่าเฉลี่ยสำหรับการแสดงออกของยีนตัวอย่างในตัวอย่างจากอวัยวะต่างๆหลังจากการรักษาด้วยยาหลายชนิด นอกจากนี้ ค่า t-test statistical significanc EP จะแสดงสำหรับความแตกต่างในการแสดงออกของยีนระหว่างตัวอย่างควบคุมและตัวอย่างที่แตกต่างกันสามตัวอย่างจากการตอบสนองของปริมาณยาที่แตกต่างกันซึ่งระบุด้วยเครื่องหมายดอกจัน โดยปกติแล้วจะมีเครื่องหมายดอกจันหนึ่งดอก ที่ตรงกับ AP - ค่าต่ำกว่า 0.05 เครื่องหมายดอก จันสองดอกที่ตรงกับ AP - ค่าต่ำกว่า 0.01 และดอกจันสามดอก ที่ตรงกับ AP - ค่าต่ำกว่า 0.001
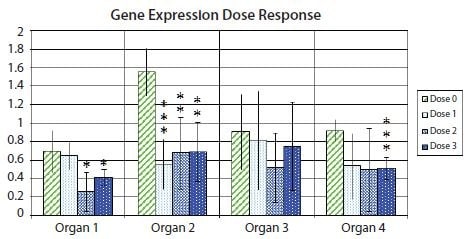
รูปที่ 10 11การเปลี่ยนแปลงการพับ (log2) การแสดงออกของยีนที่น่าสนใจที่สัมพันธ์กับคู่ของยีนอ้างอิงสัมพันธ์กับการแสดงออกในตัวอย่างที่มีการแสดงออกต่ำสุดภายในอวัยวะแต่ละชนิด ความสูงของแท่งแสดงถึงการแสดงออกของยีนในตัวอย่างหลายตัวอย่างในกลุ่มตัวอย่างที่ไม่ได้รับการรักษา (ขนาดยาที่ 1) หรือตัวอย่างที่ได้รับการรักษาด้วยยาที่แตกต่างกัน 0 ชนิด (ขนาดยาที่ 1 ขนาดยาที่ 2 และขนาดยาที่ 3) แถบค่าคลาดเคลื่อนจะระบุค่าประมาณช่วงความเชื่อมั่น 95% ของนิพจน์ค่าเฉลี่ย เครื่องหมายดอกจันหนึ่งดอกแสดงถึงส่วนต่างของนัยสำคัญทางสถิติระหว่างค่าเฉลี่ยของชุดตัวอย่างที่ได้รับการรักษาเทียบกับค่าเฉลี่ยของตัวอย่างที่ไม่ได้รับการรักษาที่ตั้งค่าไว้ที่ร้อยละ 5 เครื่องหมายดอกจันสองดอกแสดงถึงส่วนต่างของนัยสำคัญทางสถิติที่ร้อยละ 1 เครื่องหมายดอกจันสามดอกแสดงถึงส่วนต่างของนัยสำคัญทางสถิติที่ร้อยละ 0.1
เนื่องจากเครื่องหมายดอกจันซ่อนค่าสัมบูรณ์ o FPจึงมักแนะนำให้รวมตารางที่มีค่าสัมบูรณ์ o FPดังที่แสดงในตัวอย่างใน ตารางที่ 10.5 เหตุผลหนึ่งที่อยู่เบื้องหลังเรื่องนี้ก็คือ ค่า AP ของตัวอย่างเช่น 0.032 นั้น“มีนัยสำคัญ”มากกว่า ค่า AP เท่ากับ 0.055 เล็กน้อย กรณีที่มีเส้นขอบเช่นนี้อาจทำให้เกิดความสับสนในการตัดสินใจอย่างแม่นยำว่าจะใช้การตัดสิ่งใดเมื่อจัดประเภทข้อมูลให้มีความสำคัญ ในกรณีที่เป็นไป ได้จริงค่า AP ของ 0.051 อาจมีความสำคัญเท่ากับ ค่า AP ของ 0.049 แต่การตัดออกอย่างเข้มงวด (แม้ว่าโดยทั่วไป) ของ 0.05 จะจัดประเภทหนึ่งเป็นสำคัญและอื่นๆไม่ได้
อย่างไรก็ตามมีตัวแปรของการแสดงภาพแผนภูมิแท่งที่ใช้ประโยชน์จากช่วงความเชื่อมั่นของความแตกต่างระหว่างวิธีการหลีกเลี่ยงหลายถ้าไม่ทั้งหมดของข้อเสียของแผนภาพบาร์แบบดั้งเดิม24 ด้วยช่วงความเชื่อมั่นของความแตกต่างระหว่างค่าเฉลี่ยคุณสามารถประมาณค่าความสำคัญทางสถิติโดยตรงด้วยแถบค่าคลาดเคลื่อนที่เกี่ยวข้องในขณะเดียวกันก็เน้นขนาดของผลกระทบทางชีวภาพและความผันแปรของข้อมูลได้ รูปที่ 10.1 2 แสดงตัวแปรที่มีช่วงความเชื่อมั่นของความแตกต่างระหว่างวิธีการของข้อมูลที่ใช้ใน รูปที่ 10.11 โปรดสังเกตว่าช่วงความเชื่อมั่นที่ไม่ครอบคลุมความแตกต่างเป็นศูนย์ระหว่างค่าเฉลี่ยจะสอดคล้องกับผลลัพธ์ที่สำคัญในระดับความเชื่อมั่นที่สอดคล้องกับ การตัดมูลค่า EP (ร้อยละ 5 ใน รูปที่ 10.1 1 และ ตารางที่ 10.5)

รูปที่ 10 12แผนภูมิแท่งแสดงความแตกต่างระหว่างวิธีการของชุดตัวอย่างที่ไม่ได้รับการรักษา (ขนาดยา 0 และชุดตัวอย่างที่ได้รับการรักษา (ขนาดยา 1 ขนาดยา 2 11 หรือขนาดยา 3) ในชุดข้อมูลจากรูปที่ 10 แถบค่าคลาดเคลื่อนจะแสดงช่วงความเชื่อมั่นของความแตกต่างระหว่างค่าเฉลี่ย แถบค่าคลาดเคลื่อนที่ไม่ตัดกับแกน x แสดงว่าการเปรียบเทียบค่าเฉลี่ยที่สอดคล้องกันมีนัยสำคัญทางสถิติเป็น 5% ในการทดสอบแบบ t เทคโนโลยี PCR, นวัตกรรมปัจจุบัน - 3 เอ็ด. โดยเทย์เลอร์และฟรานซิสกรุ๊ป LLC หนังสือ. ทำซ้ำโดยได้รับอนุญาตจาก Taylor และ Francis Group LLC Books ในรูปแบบการนำกลับมาใช้ใหม่ในหนังสือ/หนังสืออิเล็กทรอนิกส์ผ่านศูนย์การกวาดล้างลิขสิทธิ์
ข้อมูลที่มีหลายตัวแปรจะถูกเก็บรวบรวมบนตัวแปรหลายตัวสำหรับแต่ละหน่วยการสุ่มเก็บข้อมูล ข้อมูลที่ใช้ใน รูปที่ 10.1 1 และ 10.1 2 เป็นตัวแปรที่ขึ้นอยู่กับตัวแปรเช่นขนาดและประเภทของอวัยวะ อย่างไรก็ตามการวิเคราะห์ทางสถิติในรูปที่ 10.1 1 และ 10.1 2 ยังคงเป็นแบบเดียวกันในการแสดงแต่ละ (แถบ) จะแสดงเฉพาะตัวแปรหนึ่งตัวแปรการแสดงออกของยีนที่สัมพันธ์กับการวัดคงที่ของตัวแปรอื่นๆ สำหรับเทคนิคการวิเคราะห์ข้อมูลหลายตัวแปรการจัดกลุ่มลำดับชั้นและการวิเคราะห์ส่วนประกอบหลักเป็นตัวเลือกที่ดีสำหรับการแสดงข้อมูล
การจัดกลุ่มตามลำดับชั้น
หนึ่งในวิธีที่ง่ายที่สุดและมีประโยชน์ในการกำหนดลักษณะข้อมูลคือการพล็อตข้อมูลใน scatterplot (ตัวอย่างเช่นการพล็อต ค่า Cq ที่วัดได้ของ ยีนหนึ่งกับค่า Cq ที่สอดคล้องกันของยีนอื่นสำหรับชุดของตัวอย่างทางชีวภาพในพล็อต 2 มิติ) แปลงในหนึ่งหรือสองมิติจะมองเห็นได้อย่างสะดวกด้วยตาของมนุษย์ พล็อตในสามมิติอาจเป็นไปได้ด้วยเครื่องมือที่เหมาะสมแต่พล็อตมิติที่สูงขึ้นนั้นยากที่จะมองเห็นได้ อย่างไรก็ตามสำหรับการศึกษาเชิงสำรวจชุดข้อมูลนั้นมีหลายมิติโดยเนื้อแท้และมีการแปลงข้อมูลของชุดข้อมูลทั้งหมดจึงอาจไม่สามารถใช้งานได้ จากชุดข้อมูล qPCR อาจมียีนหลายตัวและ/หรือตัวอย่างทางชีวภาพหลายชนิดที่แสดงอยู่
วิธีทางเลือกที่ได้รับความนิยมในการกำหนดลักษณะและแสดงภาพข้อมูลจากการศึกษาเชิงสำรวจคือการวิเคราะห์การวัดระยะห่างระหว่างจุดข้อมูลในการกระจายข้อมูล มีการวัดระยะทางที่แตกต่างกันรวมถึง Euclidean, Manhattan และ Pearson Correlations ด้วยพลังในการคำนวณการคำนวณระยะทางจะไม่ซับซ้อนแม้แต่ข้อมูลหลายมิติที่มีมิติสูงกว่าสามมิติ สำหรับการทำคลัสเตอร์แบบลำดับชั้นแบบ agglomerative จะมีการดำเนินการกระบวนการซ้ำต่อไปนี้: 2) ค้นหาวัตถุที่ใกล้เคียงที่สุด 1 1 รายการและรวมเข้ากับคลัสเตอร์ ; 2) กำหนดคลัสเตอร์ใหม่เป็นวัตถุใหม่ผ่านวิธีการทำคลัสเตอร์ ; 3 ทำซ้ำจาก 2) จนกว่าวัตถุทั้งหมดจะถูกรวมเข้าด้วยกันเป็นกลุ่ม30 ทางเลือกสำหรับวิธีการจัดกลุ่มรวมถึงวิธีการของวอร์ด, การเชื่อมโยงเดี่ยวและการเชื่อมโยงเฉลี่ย31 มักใช้ dendrogram เพื่อแสดงผลลัพธ์จากการจัดกลุ่มแบบลำดับชั้น
การตีความของการจัดกลุ่มลำดับชั้น dendrograms ของข้อมูล qPCR มักจะส่งผลให้เกิดข้อสรุปเกี่ยวกับความคล้ายคลึงกันของโปรไฟล์การแสดงออกของยีน ในการศึกษาเชิงสำรวจความคล้ายคลึงกันเหล่านี้อาจถูกนำมาใช้ในการกำหนดสมมติฐานเกี่ยวกับการควบคุมการแสดงออกของยีนซึ่งอาจได้รับการยอมรับหรือปฏิเสธในการศึกษายืนยันที่ตามมา ข้อดีของการจัดกลุ่มแบบลำดับชั้นของ dendrograms จะรวมถึงความชัดเจนซึ่งความสัมพันธ์ที่มีความคล้ายคลึงกันจะถูกแสดงให้เห็น ในทางกลับกันการเน้นที่มาตรการความคล้ายคลึงกันอย่างมากอาจถูกมองว่าเป็นการจำกัดเกี่ยวกับการกำหนดสมมติฐานเนื่องจากโปรไฟล์นิพจน์ที่คล้ายกันอาจเป็นคุณลักษณะที่ซ้ำซ้อนในสมมติฐาน การระบุชุดของโปรไฟล์นิพจน์ที่เสริมกันในการรวมกันที่เฉพาะเจาะจงอาจเป็นค่าที่สูงกว่าเพื่อตอบสมมติฐานที่ต้องการ
การวิเคราะห์ส่วนประกอบหลัก
อีกวิธีหนึ่งที่เป็นที่นิยมและเป็นทางเลือกในการกำหนดลักษณะและแสดงภาพข้อมูลจากการศึกษาเชิงสำรวจคือการใช้ประโยชน์จากข้อมูลที่มีอยู่ในชุดข้อมูลหลายมิติทั้งหมดเลือกคุณสมบัติที่ต้องการและฉายภาพไปยังจุดกระจายภาพมิติที่ต่ำกว่าเช่นพล็อต 2 มิติหรือ 3 มิติ ซึ่งสามารถทำได้โดยใช้การวิเคราะห์ส่วนประกอบหลัก (PCA)32 33 34 35 ในที่นี้ระบบพิกัดเดิมของชุดข้อมูล (เช่นโปรไฟล์นิพจน์ที่วัดโดย qPCR) จะถูกแปลงเป็นพื้นที่หลายมิติใหม่ที่ตัวแปรใหม่ (องค์ประกอบหลัก: PC หรือปัจจัย) ถูกสร้างขึ้น PC แต่ละเครื่องจะเป็นการรวมกันแบบเส้นตรงของซับเจกต์ในชุดข้อมูลเดิม ตามนิยามทางคณิตศาสตร์พีซีจะถูกแยกออกมาตามลำดับความสำคัญ ซึ่งหมายความว่าพีซีเครื่องแรกจะอธิบายข้อมูลส่วนใหญ่ (ความแปรปรวน) ที่มีอยู่ในข้อมูลส่วนที่สองจะน้อยลงเรื่อยๆ ดังนั้นพิกัด PC สองหรือสามพิกัดแรก (คะแนนที่เรียก) จึงสามารถใช้เพื่อรับการฉายภาพของชุดข้อมูลทั้งหมดลงในขนาดที่เล็กลงได้อย่างสะดวกเหมาะสำหรับการแสดงภาพในพล็อต 2 มิติหรือ 3 มิติ ด้วยการใช้พีซีสองหรือสามเครื่องแรกในการแสดงภาพการฉายภาพที่มีความผันแปรมากที่สุดในชุดข้อมูลจะได้รับ ความแปรปรวนจากเงื่อนไขการออกแบบทดลองคาดว่าจะเป็นระบบในขณะที่ความแปรปรวนที่สับสนคาดว่าจะเป็นแบบสุ่มดังนั้นการแสดงนี้อาจเป็นที่ต้องการภายใต้เงื่อนไขที่เหมาะสม
ดังที่ได้ระบุไว้ก่อนหน้านี้สำหรับการจัดกลุ่มตามลำดับชั้นการตีความของ qPCR PCA มักจะส่งผลให้เกิดข้อสรุปเกี่ยวกับความคล้ายคลึงกันของโปรไฟล์การแสดงออกของยีน แม้ว่า PCA และการจัดกลุ่มแบบลำดับชั้นอาจให้ข้อมูลเชิงลึกที่ส่งเสริมกันในรูปแบบการควบคุมร่วมกันของการแสดงออกของยีนแต่เทคนิคทั้งสองจะมุ่งเน้นไปที่ความคล้ายคลึงกันของโปรไฟล์การแสดงออกของยีน ซึ่งจะเป็นการจำกัดประเภทของสมมติฐานที่สามารถพบได้ในการศึกษาเชิงสำรวจโดยใช้เทคนิคเหล่านี้เพียงอย่างเดียว ในการขยายการเข้าถึงสมมติฐานที่สร้างขึ้นในการศึกษาเชิงสำรวจแนวทางที่ขับเคลื่อนด้วยสมมติฐานในการวิเคราะห์หลายตัวแปรได้รับการเสนอเมื่อเร็วๆนี้24 อัลกอริธึมที่ออกแบบตามสมมติฐานและกำหนดเองอาจระบุสมมติฐานที่เกี่ยวข้องทางชีวภาพซึ่งอาจพลาดไปจากเทคนิคที่ใช้กันทั่วไปในการวิเคราะห์ข้อมูลหลายตัวแปร
วัสดุ
เพื่ออ่านต่อ โปรดเข้าสู่ระบบหรือสร้างบัญชีใหม่
ยังไม่มีบัญชีใช่หรือไม่?